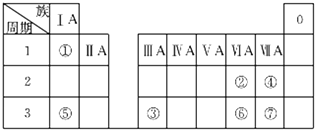
为了说明影响化学反应快慢的因素,甲、乙、丙、丁四位学生分别设计了如下A~D四个实验,你认为结论不正确的是( )
| A、将铜片放入稀硫酸中,无现象.若再向所得的溶液中加入硝酸银溶液,一段时间后,由于形成原电池,可看到有氢气产生 |
| B、在相同条件下,等质量的大理石块和大理石粉与相同的盐酸反应,大理石粉反应快 |
| C、将浓硝酸分别放在冷暗处和强光照射下,会发现光照可以加快浓硝酸的分解 |
| D、两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同 |
C+CO2?2CO(正反应吸热),反应速率为v1:N2+3H2?2NH3(正反应放热),反应速率为v2.对于上述反应,当温度降低时,v1和v2的变化情况是( )
| A、同时增大 |
| B、同时减小 |
| C、v1增加,v2减小 |
| D、v1减小,v2增大 |
已知分解1mol H2O2放出热量98kJ.在含有少量I-的溶液中,H2O2分解的机理为:H2O2+I-→H2O+IO-H2O2+IO-→H2O+O2+I-.下列有关该反应的说法正确的是( )
| A、反应速率与I-浓度有关 |
| B、IO-也是该反应的催化剂 |
| C、反应活化能等于98kJ?mol-1 |
| D、v(H2O2)=v(H2O)=v(O2) |
在一恒容密闭烧瓶中注入NO2,在25℃时建立平衡:2NO2?N2O4△H<0.若把烧瓶置于100℃的沸水中,下列情况:①颜色 ②平均摩尔质量 ③质量 ④压强 ⑤密度中不变的是( )
| A、③⑤ | B、③④ | C、②④ | D、①③ |
下列反应属于氧化还原反应的是( )
| A、CaO+H2O=Ca(OH)2 | ||||
B、CaCO3
| ||||
C、Fe2O3+3CO
| ||||
D、NH4Cl+NaOH
|
反应:PCl5(g)?PCl 3(g)+Cl2(g) ①
2HI(g)?H2(g)+I2(g) ②
2NO2(g)?N2O4(g) ③
在一定条件下,达到化学平衡时,反应物的转化率均是a%.若保持各自的温度不变、体积不变,分别再加入一定量的各自的反应物,则转化率( )
2HI(g)?H2(g)+I2(g) ②
2NO2(g)?N2O4(g) ③
在一定条件下,达到化学平衡时,反应物的转化率均是a%.若保持各自的温度不变、体积不变,分别再加入一定量的各自的反应物,则转化率( )
| A、均不变 |
| B、均增大 |
| C、①增大,②不变,③减少 |
| D、①减少,②不变,③增大 |
将BaO2放入密闭真空容器中,反应2BaO2(s)═2BaO(s)+O2(g)达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是( )
| A、平衡常数减小 |
| B、BaO量不变 |
| C、氧气压强不变 |
| D、BaO2量减少 |