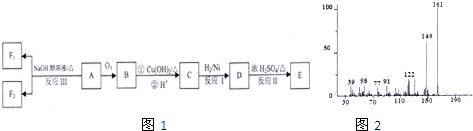
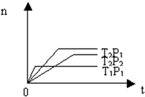
 反应2X(g)+Y(g)?2Z(g);△H<0(正反应为放热反应),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示.则下列判断正确的是( )
反应2X(g)+Y(g)?2Z(g);△H<0(正反应为放热反应),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示.则下列判断正确的是( )| A、T1<T2,P1<P2 |
| B、T1<T2,P1>P2 |
| C、T1>T2,P1>P2 |
| D、T1>T2,P1<P2 |
X、Y、Z为三种气体,把amolX和bmolY充入一密闭容器中,发生反应X+2Y?2Z.达到平衡时,若他们的物质的量满足:n(X)+n(Y)=n(Z)则Y的转化率为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
在2L的密闭容器中把4molA和2molB混合,在一定条件下发生反应3A(g)+2B(g)?zC(g)+2D(g).2min后反应达到平衡时生成1.6molC,又测得反应速率v(D)=0.2mol/(L?min).则下列说法不正确的是( )
| A、z=4 | ||
| B、B的转化率是40% | ||
| C、A的平衡浓度是1.4mol/L | ||
D、平衡时气体压强是原来的
|
在密闭容器中进行反应X2(g)+Y2(g)?2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol?L-1、0.2mol?L-1、0.2mol?L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
| A、Z为0.2 mol?L-1 |
| B、Y2为0.35 mol?L-1 |
| C、X2为0.3 mol?L-1 |
| D、Z为0.4 mol?L-1 |
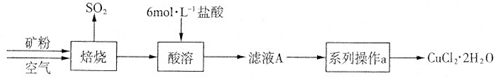
关于工业转化图(见图),下列说法不正确的是( )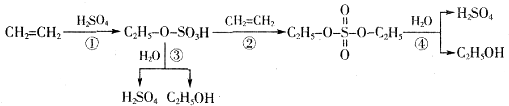

| A、该过程是一种“对环境友好型”工业生产硫酸的方法 |
| B、从以上物质的转化过程可看出硫酸可作乙烯水化法制乙醇的催化剂 |
| C、该过程中①②是加成反应 |
| D、该过程中③④是酯类的水解 |
下列物质间的转化在给定条件下能够实现的是( )
①Al2O3
NaAlO2(aq)或Na[Al(OH)4](aq)
Al(OH)3
②S
SO3
H2SO4
③NaOH(aq)
NaHCO3
Na2CO3
④Fe2O3
FeCl3(aq)
无水FeCl3
⑤NH4Cl(s)
NH3
NH4HCO3.
①Al2O3
| NaOH(aq) |
| △ |
| CO2 |
②S
| O2 |
| 点燃 |
| H2O |
③NaOH(aq)
| 足量CO2 |
| △ |
④Fe2O3
| HCl(aq) |
| △ |
⑤NH4Cl(s)
| 熟石灰 |
| △ |
| H2O、CO2 |
| A、①③⑤ | B、②③④ |
| C、②④⑤ | D、①④⑤ |
下列关于有机化合物的说法正确的是( )
| A、分子式为C3H6O2的链状有机物中含有一个双键 |
| B、1 mol甲烷与Cl2完全发生取代反应需2 mol Cl2 |
| C、1 mol乙烯与Cl2完全发生加成反应需2 mol Cl2 |
| D、乙醇与乙酸均能被酸性KmnO4溶液氧化 |
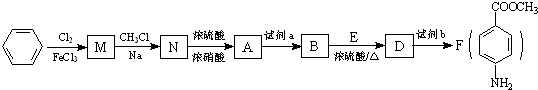
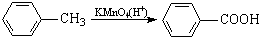


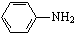 最多能够和
最多能够和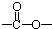 结构;
结构;