以下说法:①SO2、SiO2、CO均为酸性氧化物
②KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质
③碱性氧化物一定是金属氧化物
④硫酸、火碱、纯碱、生石灰分别属于酸、碱、盐和氧化物
⑤二氧化硅的分子式为SiO2,酸性氧化物,能与NaOH溶液反应
⑥正四面体分子中键角一定是109°28′
⑦CO2 与SiO2化学性质相似物理性质也相似
⑧福尔马林、水玻璃、氨水均为混合物
⑨强电解质溶液的导电能力一定比弱电解质溶液的导电能力强.
其中正确的是( )
②KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质
③碱性氧化物一定是金属氧化物
④硫酸、火碱、纯碱、生石灰分别属于酸、碱、盐和氧化物
⑤二氧化硅的分子式为SiO2,酸性氧化物,能与NaOH溶液反应
⑥正四面体分子中键角一定是109°28′
⑦CO2 与SiO2化学性质相似物理性质也相似
⑧福尔马林、水玻璃、氨水均为混合物
⑨强电解质溶液的导电能力一定比弱电解质溶液的导电能力强.
其中正确的是( )
| A、①③④⑤⑥ | B、④⑥⑧⑨ |
| C、③④⑧ | D、②④⑦⑨ |
下列关于酸、碱、盐、氧化物的元素组成的说法中,正确的是( )
| A、酸、碱一定含有氢,盐一定不含氢 |
| B、碱、盐可能含氧,酸一定含氧 |
| C、酸、碱、盐可能都不含金属元素 |
| D、金属氧化物一定是碱性氧化物 |
往NH4HSO4溶液中逐滴加入Ba(OH)2溶液,可能发生的离子方程式正确的是( )
| A、Ba2++SO42-=BaSO4↓ |
| B、NH4++H++2OH-=NH3?H2O+H2O |
| C、NH4++H++SO42-+Ba2++2OH-=BaSO4↓+NH3?H2O+H2O |
| D、NH4++H++2SO42-+2Ba2++2OH-=2BaSO4↓+NH3?H2O+H2O |
下列有关物质的表达式正确的是( )
| A、乙酸乙酯的结构简式:CH3CH2COOCH3 |
B、2-甲基-2-戊烯的键线式: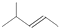 |
| C、乙醇的结构简式:CH3CH2OH |
| D、1,3-丁二烯的分子式:C4H8 |
美国科学家将两种元素铅和氪的原子核对撞,获得了一种质子数为118、中子数为175的超重元素,该元素中子数与核外电子数之差是( )
| A、57 | B、47 | C、64 | D、293 |
在核反应方程
He+
N→
O+X中,X代表的粒子是( )
4 2 |
14 7 |
17 8 |
A、
| ||
B、
| ||
C、
| ||
D、
|
对由X、Y元素形成的化合物X2Y2的叙述正确的是( )
| A、若是离子化合物,则阳阴离子个数比肯定不等于1:1 |
| B、若该化合物有Y-Y键,则肯定是共价化合物 |
| C、若溶于水时有X-Y键的断裂,则肯定是强电解质 |
| D、若X、Y原子间的共价键键能大,则熔、沸点肯定高 |
下列各项比较中前者高于(或大于或强于)后者的是( )
| A、CCl4和SiCl4的熔点 |
| B、I2在水中的溶解度和I2在CCl4溶液中的溶解度 |
C、对羟基苯甲醛(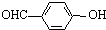 )和邻羟基苯甲醛( )和邻羟基苯甲醛(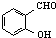 )的沸点 )的沸点 |
| D、H2SO3和H2SO4的酸性 |
当温度达到374℃,压强为2.2×104KPa时,水处于超临界状态,此时水具有较高浓度的H+和OH-,能溶解更多的有机物质,下列对临界状态水的推测正确的是( )
| A、超临界水的pH较常温时升高 |
| B、超临界水的离子积增大 |
| C、超临界水发生了化学变化 |
| D、大多数有机物在超临界水中溶解度更小 |
在一个固定容积的密闭容器中,可逆反应:mA(g)+nB(g)?pC(g)+qD(g)中,当m、n、p、q为任意正整数时,达到平衡的标志是( )
| A、体系压强不再发生变化 |
| B、各组分的物质的量浓度不再改变 |
| C、各组分的质量分数不再改变 |
| D、反应速率vA:vB:vC:vD=m:m:p:q |