设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、1L0.1mol?L-1的氨水中有0.1NA个NH4+ |
| B、标准状况下,22.4L盐酸含有NA个HCl分子 |
| C、常温常压下,14g由N2与CO组成的混合气体含有的原子数目为0.5NA |
| D、标准状况下,6.72LNO2与水充分反应转移的电子数目为0.2NA |
NA表示阿伏加德罗常数,下列说法正确的是( )
| A、25℃时,2LpH=1的H2SO4溶液中,SO42-数目为0.1NA | ||
| B、300 mL 2 mol/L蔗糖溶液中所含分子数为0.6 NA | ||
C、标准状况下,V L CHCl3含有的碳原子数为
| ||
| D、1 mol OH-参与电解,反应过程中转移的电子数为NA |
设NA表示阿伏加德罗常数,下列说法正确的是( )
| A、1L 1mol/L的FeCl3液中含Fe3+的数目为NA |
| B、室温下,21.0g乙烯和丁烯的混合气体中含有的子数目为1.5NA |
| C、标准状况下,2.24LCl2与足量稀NaOH溶液反应,转移的电子总数为0.2NA |
| D、18gNH4-中含有的质子数为0.1NA |
设NA为阿伏加德罗常数的值,下列说法中正确的是( )
| A、6.0g金刚石中含有的共价键数为NA |
| B、56g铁粉与酸反应失去的电子数一定为0.2 NA |
| C、1 mol?L-1AlCl3溶液中含有3NA个Cl |
| D、标况下,11.2LSO3所含的分子数为0.5NA |
由14CO和12CO组成的混合气体与同温同压下空气的密度相等(空气的平均相对分子质量为29,)则下列关系正确的是( )
| A、混合气体中,12CO占有的体积大于14CO占有的体积 |
| B、混合气体中,12CO与14CO分子个数比为1:2 |
| C、混合气体中,12CO与14CO质量比为15:14 |
| D、混合气体中,12CO与14CO密度比为14:15 |
下列有关化学用语使用正确的是( )
A、N2的电子式: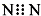 | ||
B、中子数为18的氯原子结构示意图: | ||
C、质子数为53,中子数为78的碘原子:
| ||
| D、NaHCO3在水溶液中的电离方程式:NaHCO3 ═Na++H++CO32- |
对下列氧化还原反应中转移电子数的判断,不正确的是( )
| A、H2S+H2SO4(浓)=S↓+SO2↑+2H2O:6e- |
| B、3Cl2+6KOH5KCl+KClO3+3H2O:5e- |
| C、2Na2O2+2H2O=4NaOH+O2↑:2e- |
| D、2H2S+SO2=3S+2H2O:4e- |
已知CH4、H2O和NH3的物质的量均为1mol,下列说法不正确的是( )
| A、所含分子数之比为1:1:1 |
| B、所含氢原子数之比为4:2:3 |
| C、摩尔质量之比为1:1:1 |
| D、质量之比为16:18:17 |
在一定温度和压强下,将装有N2和NO2混合气体的试管倒立于水槽中,最后试管内气体的体积缩小为原体积的
,则混合气体中N2与NO2的体积比是( )
| 3 |
| 5 |
| A、2:3 | B、3:2 |
| C、3:5 | D、5:3 |