PCl3和PCl5都是重要的化工原料.将PCl3(g) 和Cl2(g)充入体积不变的2 L密闭容器中,在一定条件下发生下述反应,并于10 min时达到平衡:PCl3(g)+Cl3(g)?PCl3(g).有关数据如下:
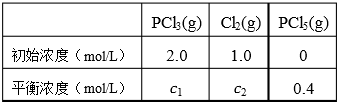
下列判断不正确的是( )

下列判断不正确的是( )
| A、10 min内,v(Cl2)=0.04 mol/(L?min) |
| B、当容器中Cl2为1.2 mol时,反应达到平衡 |
| C、升高温度(T1<T2),反应的平衡常数减小,平衡时PCl3的转化率变大 |
| D、平衡后移走2.0 mol PCl3和1.0 molCl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol/L |
对于可逆反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列正确的是( )
A、平衡常数的表达式K=
| ||
| B、当v正(NH3):v正(NO)=1:1时,说明该反应已经达到平衡 | ||
| C、若平衡时两种反应物的转化率相等,则起始投入的n(NH3):n(O2)=5:4 | ||
| D、反应达到平衡后,恒容条件下,同倍数改变NH3和NO的量,c(O2)=可能不变 |
在相同温度下,先在1L密闭容器中充入1mol H2(g)和1mol 的I2(g),发生反应 H2(g)+I2(g)?2HI(g);再在2L的另一密闭容器中充入1mol HI(g),发生反应:HI(g)?
H2(g)+
I2(g),达到平衡时,两容器中HI的体积分数为50%,则两者的平衡常数( )
| 1 |
| 2 |
| 1 |
| 2 |
| A、前者大 | B、前者小 |
| C、相等 | D、无法比较 |
不能用于区别稀硫酸和浓硫酸的方法的是( )
| A、加水溶解,观察溶液温度变化 |
| B、取相同质量敞口放置,过一段时间在称量,比较质量变化 |
| C、取相同量,加入到氯化钡溶液中,观察是否有沉淀产生 |
| D、取相同量于试管中,加入铜片,加热观察,是否有刺激性气味的气体产生 |
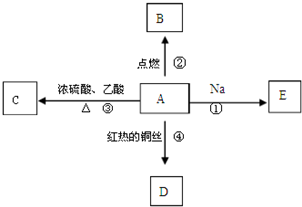 A是乙醇的同系物,其分子中只有1个甲基,相对分子质量为60,它能进行如图所示的多种反应:
A是乙醇的同系物,其分子中只有1个甲基,相对分子质量为60,它能进行如图所示的多种反应: