下列叙述中正确的是( )
| A、在稀溶液中,1mol酸和1mol碱完全反应所放出的热量,叫作中和热 |
| B、在101kpa时,1mol物质燃烧时所放出的热量叫作该物质的燃烧热 |
| C、热化学方程式中,各物质前的化学计量数不表示分子个数 |
| D、已知S(s)+O2(g)=SO2(g)△H1;S(g)+O2(g)=SO2(g)△H2,则△H1<△H2 |
下列电离或水解方程式正确的是( )
| A、Na2SO3的水解:SO3 2-+2H2O?H2SO3+2OH- |
| B、NaHCO3的电离:NaHCO3?Na++H++CO3 2- |
| C、KHS的电离:KHS=K++HS- |
| D、NaClO溶液与FeCl2溶液混合:2ClO-+Fe2++2H2O=2HClO+Fe(OH)2↓ |
下列热化学方程式正确的是( )
| A、甲烷的燃烧热为890.3 kJ?mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ?mol-1 | |||
| B、500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为 N2(g)+3H2(g)
| |||
C、已知在101 kPa下,1 g H2燃烧生成水蒸气放出121 kJ热量,其热化学方程式为H2(g)+
| |||
| D、25℃,101 kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ?mol-1,硫酸溶液与氢氧化钾溶液反应的中和热的热化学方程式为H2SO4(aq)+2KOH(aq)═K2SO4(aq)+2H2O(l)△H=-114.6 kJ?mol-1 |
我国镍氢电池居世界先进水平.常见镍氢电池的某极是储氢合金LaNi5H6 (LaNi5H6中各元素化合价均为零),电池反应通常表示为LaNi5H6+6NiO(OH)?LaNi5+6Ni(OH)2,下列说法正确的是( )
| A、放电时储氢合金作正极 |
| B、充电时阳极周围c(OH-)增大 |
| C、放电时负极反应:LaNi5H6+6OH--6e-=LaNi5+6H2O |
| D、充电时储氢合金作阳极 |
用0.20mol/L的NaOH溶液滴定100.0mL0.20mol/LHCl溶液时,滴定误差在±0.1%以内,反应完毕后溶液的pH变化范围是( )
| A、5~9 |
| B、4.0~10.0 |
| C、4.3~9.7 |
| D、以上都不正确 |
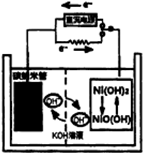 一种碳纳米管(氢气)二次电池原理如图.该电池的电解质为6moI/L KOH溶液,下列说法正确的是( )
一种碳纳米管(氢气)二次电池原理如图.该电池的电解质为6moI/L KOH溶液,下列说法正确的是( )| A、储存H2的碳纳米管放电时为负极,充电时为阳极 |
| B、充电时阳极反应为NiO(OH)+H2O+e-=Ni(OH)2+OH- |
| C、放电时正极附近溶液的pH减小 |
| D、放电时负极反应为H2+2OH--2e-=2H2O |
HCN无色有杏仁气味的有毒气体,早期广泛用于船舱、仓库的烟熏灭鼠.已知:HCN( aq)与NaOH(aq)反应的焓变△H=-12.1kJ?mol-1; HCl(aq)与NaOH(aq)反应的焓变△H=-55.6kJ?mol-1.则HCN在水溶液中电离的焓变△H等于( )
| A、-67.7 kJ?mol-1 |
| B、-43.5 kJ?mol-1 |
| C、+43.5 kJ?mol-1 |
| D、+67.7 kJ?mol-1 |
 纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的四种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的四种方法:
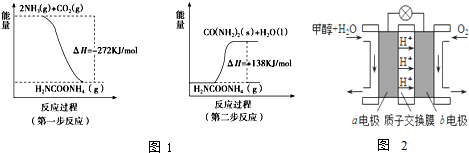
 观察图a和图b,根据盖斯定律,写出△H1、△H2、△H3、△H4、△H5和△H6的关系.
观察图a和图b,根据盖斯定律,写出△H1、△H2、△H3、△H4、△H5和△H6的关系.