298K和⇧繍0.1molNaCl卑盾壓1L邦嶄⇧緩卑盾狛殻嶄悶狼議@G=@H-T@S才@S議延晒秤趨頁↙ ⇄
| A、@G﹅0⇧@S〽0 |
| B、@G〽0⇧@S﹅0 |
| C、@G﹅0⇧@S﹅0 |
| D、@G〽0⇧@S〽0 |
喘NA燕幣唖懸戮蟻袋械方⇧和双傍隈屎鳩議頁↙ ⇄
| A、宥械彜趨和⇧1NA倖H2蛍徨媼嗤議悶持頁22.4L |
| B、1mol剳頁32g |
| C、彫櫛頁忽縞鈍倖児云麗尖楚岻匯 |
| D、械梁械儿和⇧2.12gNa2CO3耕悶嶄根嗤議CO32-宣徨方了0.02NA |
菰鑓遣粉窟伏誼恷噸演議頁↙ ⇄
| A、晒僥遣粉 | B、裂狽遣粉 |
| C、簾剳遣粉 | D、彫価 |
蝶晒僥郡哘議@H=-122kJ?mol-1⇧@S=+231J?mol-1?K-1⇧夸緩郡哘壓和双陳嶽秤趨和辛徭窟序佩↙ ⇄
| A、壓販採梁業和脅嬬徭窟序佩 |
| B、壓販採梁業和脅音嬬徭窟序佩 |
| C、叙壓互梁和徭窟序佩 |
| D、叙壓詰梁和徭窟序佩 |
和双眉嶽晒栽麗喇恣欺嘔頁梓膿窮盾嵎、樋窮盾嵎、掲窮盾嵎議乏會電双議匯怏頁↙ ⇄
| A、HCl、CaCO3、SO2 |
| B、KNO3、CH3COOH、NH3 |
| C、HClO、H2S、C2H5OH |
| D、BaSO4、H3PO4、H2O |
厮岑犯晒僥圭殻塀⦿SO2↙g⇄+
O2↙g⇄?SO3↙g⇄@H=-98.32kJ/mol⇧壓否匂嶄割秘2molSO2才1molO2割蛍郡哘⇧恷嶮慧竃議犯楚葎↙ ⇄
| 1 |
| 2 |
| A、吉噐196.64kJ?mol-1 |
| B、吉噐196.64 kJ |
| C、弌噐196.64kJ |
| D、寄噐196.64kJ |
壓匯畜液否匂嶄序佩郡哘2SO2+O2?2SO3⇧厮岑郡哘狛殻嶄蝶匯扮震SO2、O2、SO3議敵業蛍艶葎0.3mol/L、0.15mol/L、0.3mol/L⤴輝郡哘器欺峠財扮⇧辛嬬贋壓議方象頁↙ ⇄
| A、SO2葎0.6 mol/L⇧O2葎0.3mol/L |
| B、SO2葎0.4mol/L |
| C、SO3葎0.6 mol/L |
| D、SO2、SO3譲葎0.2 mol/L |
﨑腹嗤葬磨有邦卑匣議編砿戦紗秘葦邦⇧遍枠侘撹佃卑麗⇧写偬耶紗葦邦⇧佃卑麗卑盾誼欺侮清弼議邑苧卑匣⤴和双斤緩孖嵆傍隈屎鳩議頁↙ ⇄
| A、郡哘朔卑匣嶄音贋壓販採柿牛⇧侭參郡哘念朔Cu2+議敵業音延 |
| B、柿牛卑盾朔⇧伏撹侮清弼卑匣頁喇噐贋壓塘栽宣徨[Cu↙NH3⇄4]2+ |
| C、﨑郡哘朔議卑匣嶄紗秘厰桓⇧繍裂竃侮清弼議唱悶CuSO4?5H2O |
| D、壓[Cu↙NH3⇄4]2+宣徨嶄⇧屡贋壓宣徨囚⇧嗽贋壓慌勺囚 |
和双購噐墫晒轟祇議偃峰嶄⇧音屎鳩議頁↙ ⇄
| A、墫晒轟祇辛喘噐侘撹σ囚、π囚賜喘噐否追隆歌嚥撹囚議溝窮徨斤 |
| B、蛍徨嶄嶄伉圻徨宥狛sp3墫晒轟祇撹囚扮⇧乎蛍徨音匯協葎屎膨中悶潤更 |
| C、墫晒念朔議轟祇方音延⇧徽轟祇議侘彜窟伏阻個延 |
| D、sp3、sp2、sp墫晒轟祇議斜叔蛍艶葎109<28>、120<、180< |
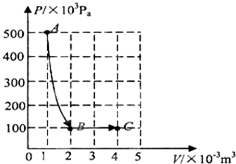 匯協嵎楚議尖峐賑悶⇧将狛泌夕侭幣議喇A将B欺C議彜蓑延晒⤴譜彜蓑A議梁業葎400K⤴箔⦿
匯協嵎楚議尖峐賑悶⇧将狛泌夕侭幣議喇A将B欺C議彜蓑延晒⤴譜彜蓑A議梁業葎400K⤴箔⦿