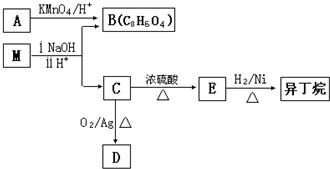
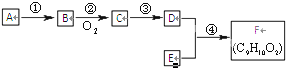
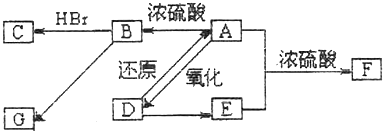
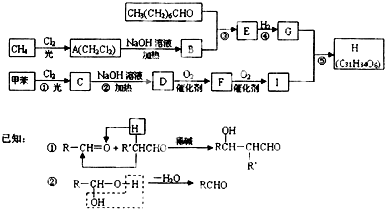
两种气态烃的混合气体共0.5mol,在空气中燃烧得到0.8mol二氧化碳和18g水,关于该混合气体的说法合理的是( )
| A、一定含甲烷,不含乙烷 |
| B、一定含乙烷,不含甲烷 |
| C、一定是甲烷和乙烯的混合物 |
| D、一定含甲烷,不含乙烯 |
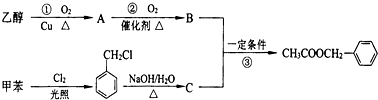
2012年3月29日,武汉大学张俐娜教授因对“纤维素低温溶解”的开创性研究,获得2011年度安塞姆佩恩奖(国际上纤维素与可再生资源材料领域的最高奖).制备乙酸乙酯的绿色合成路线之一为:
下列说法不正确的是( )

下列说法不正确的是( )
| A、M的分子式为C6H12O6 |
| B、N的结构简式为CH3COOH |
| C、M可以发生水解反应 |
| D、乙酸乙酯和N均能和NaOH溶液发生反应 |