常温下,经测定某溶液中离子只有Na+、CH3COO-、H+、OH-四种,且离子浓度大小的排列顺序为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-).其可能的情形是( )
| A、该溶液中由水电离的c(H + ) 一定小于 10 -7 mol/L |
| B、该溶液由0.1 mol?L-1的CH3COOH溶液与等物质的量浓度、等体积的NaOH溶液混合而成 |
| C、该溶液中的溶质可能是CH3COOH和CH3COONa |
| D、在上述溶液中加入适量盐酸,可使溶液中离子浓度改变为c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
实验中的下列操作正确的是( )
| A、用试管取出Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 |
| B、Ba(NO3)2 溶于水,可将含有Ba(NO3)2 的废液倒入水槽中,再用水冲入下水道 |
| C、用蒸发方法使NaCl 从溶液中析出时,应将蒸发皿中NaCl 溶液全部加热蒸干 |
| D、用药匙或者纸槽把粉末状药品送入试管的底部 |
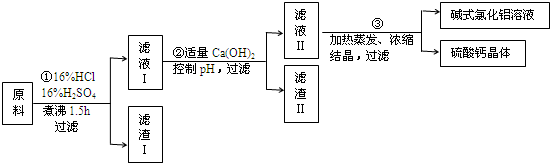
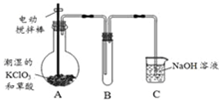 二氧化氯(ClO2)在常温下是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水.工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得.某学生拟用如图所示装置模拟工业制取并收集ClO2.
二氧化氯(ClO2)在常温下是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水.工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得.某学生拟用如图所示装置模拟工业制取并收集ClO2.