下列离子方程式正确的是( )
| A、明矾溶液与氢氧化钡溶液反应使SO42-恰好沉淀完全:SO42-+Ba2+═BaSO4↓ |
| B、将Na2CO3溶于水,溶液呈碱性:CO32-+H2O═HCO3-+OH- |
| C、次氯酸钙溶液中通入过量二氧化碳:ClO-+CO2+H2O═HCO3-+HClO |
| D、在酸性高锰酸钾溶液中滴加双氧水后产生气体:H2O2+2MnO4-+6H2O═2Mn2++3O2↑+4H2O |
下列离子方程式中,正确的是( )
| A、氯化铝溶液中加入过量的氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| B、将铜屑加入Fe3+溶液中:2Fe3++Cu═2Fe2++Cu2+ |
| C、向硫酸氢钠溶液中滴入氢氧化钡溶液至中性H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| D、石灰乳与Na2CO3溶液混合:Ca2++CO32-=CaCO3 |
在密闭容器中存在下列平衡:CaCO3(s)?CaO(s)+CO2(g),CO2的平衡浓度为C1mol/L,现再充入CO2使其浓度达到2C1mol/L,重新达到平衡后,CO2的浓度为C2mol/L(设温度不变),则C1和C2的关系是( )
| A、C1<C2 |
| B、C1=C2 |
| C、C1>C2 |
| D、2C1=C2 |
2SO2(g)+O2(g)?2SO3(g)△H<0是制备硫酸的重要反应.下列叙述正确的是( )
| A、选用有效的催化剂能增大正反应速率并提高SO2的转化率 | ||
| B、增大反应体系的压强,反应速率不一定增大 | ||
| C、该反应是放热反应,降低温度将缩短反应达到平衡的时间 | ||
D、在t1、t2时刻,SO3(g)的浓度分别是c1、c2,则时间间隔t1~t2内,SO3(g)生成的平均速率为v=
|
在化学平衡状态的体系中,如果下列物理量发生变化,其中一定能表明平衡移动的是( )
| A、反应物的转化率 |
| B、反应混和物的浓度 |
| C、正、逆反应速率 |
| D、反应混和物的压强 |
对气体反应:mA+nB?eC 温度(T)、压强(P)、时间(t)与生成物的体积百分数C%的关系图,下列结论正确的是( )


| A、正反应是放热反应 |
| B、m+n<e |
| C、T3>T4 |
| D、T1>T2 |
下列反应的离子方程式书写正确的是( )
| A、饱和石灰水与稀硝酸反应:Ca(OH)2+2H+═Ca2++2H2O |
| B、稀硫酸与锌反应:H2SO4+Zn═Zn2++SO42++H2↑ |
| C、碳酸钙与稀硫酸反应:CaCO3+2H+═Ca2++CO2↑+H2O |
| D、小苏打溶液与NaOH反应:HCO3-+OH-═H2O+CO32- |
现用氯水来制取含有次氯酸的溶液,既要提高溶液中HClO物质的量浓度,又要降低溶液中HCl浓度,下列措施可以采用的是( )
| A、加热挥发HCl |
| B、加水使平衡向正反应方向移动 |
| C、加NaOH固体 |
| D、加CaCO3 固体 |
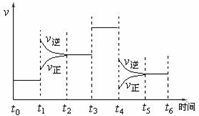 某一容积可变的密闭体系中发生下列反应:N2(g)+3H2(g)?2NH3(g)△H<0,回答下列问题:
某一容积可变的密闭体系中发生下列反应:N2(g)+3H2(g)?2NH3(g)△H<0,回答下列问题: