常温下,下列溶液中各离子浓度关系正确的是( )
| A、等物质的量的氨水和盐酸混合后的溶液:c(H+)=c(OH-)+c(NH3?H2O) |
| B、浓度为0.1 mol?L-1的碳酸钠溶液:c(Na+)=2c(CO32-)+c(HCO3-)+c(H2CO3) |
| C、将pH=3的盐酸溶液和pH=11的氨水等体积混合:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D、醋酸溶液与NaOH溶液相混合后,所得溶液呈中性:c(Na+)>c(CH3COO-) |
有关离子浓度大小比较的判断正确的是( )
| A、常温下NaB溶液的pH=8,c(Na+)-c(B-)=1×10-2 mol/L |
| B、Na2CO3溶液中,2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| C、KHSO3溶液呈酸性,c(K+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-) |
| D、0.1mol?L-1 NH4Cl和0.1mol?L-1 NH3?H2O等体积混合后溶液呈碱性:c(NH3?H2O)>c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
将0.2mol?L-1MOH溶液和0.1mol?L-1HCl的溶液等体积混合后,溶液呈酸性,下列关系式中不正确的是( )
| A、c(MOH)>c(M+) |
| B、c(M+)+c(H+)=c(Cl-)+c(OH-) |
| C、c(MOH)+c(M+)=0.2mol?L-1 |
| D、c(M+)<c(Cl-) |
下列条件下的水溶液中,离子一定能大量共存或符合该水溶液条件的是( )
| A、无色溶液中:K+、H+、SO42-、MnO4- |
| B、c(H+):c(OH-)=10-10的溶液中:K+、Na+、CO32-、AlO2- |
| C、c(H+):c(OH-)=1溶液中:K+、Na+、NO3-、ClO- |
| D、能使pH试纸变蓝色的溶液中:Ca2+、Na+、CO32-、SO42- |
X、Y、Z、W四块金属分别用导线两两相连浸入稀硫酸中组成原电池,X、Y相连时,X为负极;Z、W相连时,电流方向是W→Z;X、Z相连时,Z极上产生大量气泡;W、Y相连时,W极发生氧化反应.据此判断金属的活动性顺序是( )
| A、Y>W>Z>X |
| B、X>Z>W>Y |
| C、Z>X>Y>W |
| D、X>Y>Z>W |
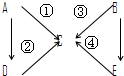 如图表示A-E五种含氮物质相互转化的关系图.其中A、B、C、D常温下都是气体,B为红棕色.
如图表示A-E五种含氮物质相互转化的关系图.其中A、B、C、D常温下都是气体,B为红棕色.(1)写出下列物质的化学式:A
(2)各步反应的化学方程式:
①

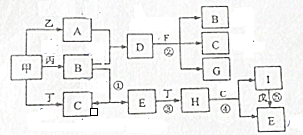
 氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用.
氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用.