下列说法中,正确的是( )
| A、同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同 | ||||
B、用铜作电极电解稀硫酸,反应Cu+H2SO4
| ||||
| C、铅蓄电池放电时的负极和充电时的阳极均发生还原反应 | ||||
| D、使用催化剂,可加快反应速率,改变反应限度 |
已知反应:①101kPa时,2C(s)+O2(g)=2CO(g)△H=-221kJ?mol-1 ②稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ?mol-1,下列结论正确的是( )
| A、反应①为放热反应 |
| B、碳的燃烧热大于110.5 kJ?mol-1 |
| C、浓硫酸和NaOH反应的中和热为-57.3 kJ?mol-1 |
| D、稀醋酸与稀NaOH反应生成1mol水,放出57.3 kJ的热量 |
与22g二氧化碳所含氧原子数相等的水的质量是( )
| A、9g | B、22g |
| C、44 g | D、18g |
在铁的吸氧腐蚀中,发生还原反应的那个电极上进行的电极反应是( )
| A、O2+2H2O+4e-=4OH- |
| B、2H++2e=H2↑ |
| C、4 OH-=2H2O+O2+4e- |
| D、Fe=Fe2++2e- |
SF6是一种优良的绝缘气体材料,分子结构中只存在S-F键.已知:1molS(s)转化为气态硫原子时吸收能量280kJ,形成1molF-F、S-F键需放出的能量分别为160kJ、330kJ.则S(s)+3F2(g)=SF6(g)的反应热△H为( )
| A、-720kJ/mol |
| B、+430kJ/mol |
| C、-450kJ/mol |
| D、-1220kJ/mol |
下列说法正确的是( )
| A、HClO是强酸 |
| B、根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液 |
| C、Fe在足量Cl2中燃烧只生成FeCl3 |
| D、二氧化硅是将太阳能转化为电能的常用材料 |
下列化学方程式或离子方程式正确的是( )
| A、常温下,将铁片置于浓硝酸中:Fe+6HNO3=Fe(NO3)3+3NO2↑+3H2O |
| B、向碳酸氢钠溶液中加入少量盐酸:CO32-+2H+═CO2↑+H2O |
| C、向(NH4)2SO4溶液中加入适量Ba(OH)2:Ba2++SO42-=BaSO4↓ |
| D、向浓硝酸中加入铜片:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O |
下列说法中不正确的是( )
| A、蓄电池在放电过程中,负极质量增加,正极质量也增加 |
| B、电解法是最强有力的氧化还原手段,可以将极难还原的活泼金属从它们的化合物中还原出来 |
| C、钢铁发生吸氧腐蚀时,负极反应式为:Fe-3e-═Fe3+ |
| D、电解精炼铜时,用纯铜板作阴极,粗作阳极,用硫酸铜溶液作电解液铜板 |
将1mol的X2和Y2置于一密闭容器中,在一定条件下发生反应mX2(g)+nY2(g)═pZ(g),在某一时刻,测得容器中C(X2)=0.4mol?L-1,C(Y2)=0.2mol?L-1,C(Z)=0.4mol?L-1,则Z的化学式可能是( )
| A、X2Y3 |
| B、XY3 |
| C、X2Y2 |
| D、X3Y4 |
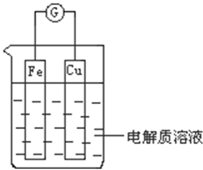 能量是一个世界性的话题,如何充分利用能量、开发新能源,为人类服务是广大科技工作者不懈努力的目标.
能量是一个世界性的话题,如何充分利用能量、开发新能源,为人类服务是广大科技工作者不懈努力的目标.