下列表示正确的是( )
A、N2的电子式: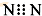 |
B、CS2分子的球棍模型: |
C、邻羟基苯甲酸的结构简式: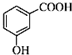 |
D、苯的比例模型: |
下列叙述正确的是( )
| A、二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
| B、某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I- |
| C、向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体 |
| D、将SO2通入品红溶液,溶液褪色后加热恢复原色,将SO2通入溴水,溴水褪色后加热也能恢复原色 |
下面不是化学方法处理污水的是( )
| A、过滤法 | B、混凝法 |
| C、中和法 | D、沉淀法 |
下列固体投入盐酸中,没有气体产生的是( )
| A、Na |
| B、Na2O |
| C、Na2O2 |
| D、Na2CO3 |
一定温度下可逆反应:A(s)+2B(g)?2C(g)+D(g)△H<0.现将1mol A和2mol B加入甲容器中,将4mol C和2mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动).下列说法正确的是( )


| A、保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均增大 |
| B、保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 |
| C、保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
| D、保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 |