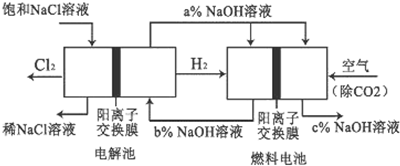
下列说法正确的是( )
| A、水的离子积常数KW只与温度有关,但外加酸、碱、盐一定会影响水的电离程度 | ||||
| B、根据HClO的Ka=3.0×10-8,H2CO3的Ka1=4.3×10-7,Ka2=5.6×10-11,可推测相同状况下,等浓度的NaClO与Na2CO3溶液中,pH前者大于后者 | ||||
C、常温下,在0.10 mol?L-1的NH3?H2O溶液中加入少量NH4Cl晶体,能使溶液的pH减小,
| ||||
| D、室温下,CH3COOH的Ka=1.7×10-5,NH3?H2O的Kb=1.7×10-5,CH3COOH溶液中的c(H+)与NH3?H2O中的c(OH-)相等 |
下列实验操作及结论都正确的是( )
| A、制取氢氧化铁胶体,可向沸水中加入FeCl3溶液 |
| B、加热蒸发NaHCO3溶液,最终可获得NaOH固体 |
| C、向醋酸溶液中加入固体的醋酸钠,可增大醋酸的电离度 |
| D、配制SnCl2溶液时,可加入过量的硫酸,抑制水解 |
对可逆反应4A(g)+5B(g)?4C(g)+6D(g)△H>0,下列叙述中,正确的是( )
| A、化学反应速率关系是:2v正(A)=3v正(D) |
| B、若单位时间内生成x mol C的同时,消耗x mol A,则反应一定处于平衡状态 |
| C、达到化学平衡后,增大容器的容积,则正反应速率减小,逆反应速率增大 |
| D、达到化学平衡后,升高温度,则C的质量分数增大 |
已知,常温下,Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.3×10-17,下列叙述中正确的是( )
| A、常温下,AgCl在饱和NaCl溶液中的Ksp比在纯水中的Ksp小 |
| B、向AgCl的悬浊液中加入0.1 mol?L-1KI溶液,沉淀可由白色转化为黄色 |
| C、将0.001 mol?L-1的AgNO3溶液滴入KCl和KI的混合溶液中,一定先产生AgI沉淀 |
| D、向AgCl的饱和溶液中加入NaCl晶体,有AgCl析出且溶液中c(Ag+)=c(Cl-) |
向溴化铁溶液中加入足量新制氯水,将溶液蒸干并充分灼烧,最后得到的固体是( )
| A、Fe2O3 |
| B、FeCl3 |
| C、FeCl3和Br2 |
| D、Fe(OH)3 |
下列说法正确的是( )
| A、凡能导电的物质一定是单质 |
| B、金属单质都能与稀硫酸发生置换反应 |
| C、活泼金属都能从盐溶液中置换出较不活泼的金属 |
| D、在化学反应中,金属单质失电子,常作还原剂 |
 在如图中,甲烧杯中盛有100mL 0.50mol?L-1 AgNO3溶液,乙烧杯中盛有100mL 0.25mol?L-1 CuCl2溶液,A、B、C、D均为质量相同的石墨电极,如果电解一段时间后,发现A极比C极重1.52g,则
在如图中,甲烧杯中盛有100mL 0.50mol?L-1 AgNO3溶液,乙烧杯中盛有100mL 0.25mol?L-1 CuCl2溶液,A、B、C、D均为质量相同的石墨电极,如果电解一段时间后,发现A极比C极重1.52g,则