设NA 表示阿伏加德罗常数的值.下列说法正确的是( )
| A、标准状况下,22.4LCH2Cl2中含C-Cl键数目为0.2NA |
| B、常温常压下,10g92%酒精水溶液含氧原子总数为0.2NA |
| C、常温常压下,0.1molNa2O2与水完全反应转移电子数为0.2NA |
| D、常温常压下,3.0g尿素与乙酸的混合物,含氢原子总数为0.2NA |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、18gH2O含有10 NA个质子 |
| B、1mol己烷含有18NA个化学键 |
| C、22.4L氨水含有NA个NH3分子 |
| D、56g铁片投入足量浓H2SO4中生成NA个SO2分子 |
设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A、0.1 mol?L-1的NaHCO3 溶液中含有Na+的数目为0.1NA |
| B、标准状况下,1mol苯含有C=C 双键的数目为3NA |
| C、常温常压下,14 g 由N2与CO组成的混合气体含有的原子数目为NA |
| D、标准状况下,22.4L NO2与水充分反应转移的电子数目为0.1NA |
根据如图示判断下列叙述符合事实的是( )
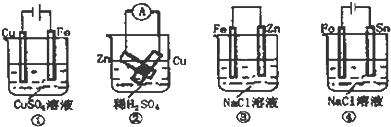

| A、按图①连接并放置一段时间后,Fe片表面会“镀”上一层铜 |
| B、按图②连接好导线后(Zn片与Cu片相接触),灵敏电流表会发生非常明显的偏转 |
| C、按图③连接并放置片刻,在Fe片附近加一滴KSCN溶液,溶液变为深红色 |
| D、按图④连接并放置一段时间后,在Sn片上有无色气泡聚集 |
NA代表阿伏加德罗常数,下列叙述错误的是( )
| A、10mL质量分数为98%的H2SO4,用水稀释至100mL,H2SO4的质量分数大于9.8% |
| B、在H2O2+Cl2=2HCl+O2反应中,每生成32g氧气,则转移电子个数为2moL |
| C、标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g |
| D、某无色溶液中通入Cl2,溶液变为棕黄色,再加入淀粉溶液,溶液变为蓝色,说明原溶液中存在I- |
下列物质属于纯净物的是( )
| A、稀硫酸 | B、NaOH |
| C、液化石油气 | D、天然气 |
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用.锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)
Zn(OH)2(s)+Mn2O3(s) 下列说法错误的是( )
| 放电 |
| 通电 |
| A、电池工作时,锌失去电子 |
| B、电池正极的电极反应式为:2MnO2(s)+H2O(1)+2e-=Mn2O3(s)+2OH-(aq) |
| C、电池工作时,电子由正极通过外电路流向负极 |
| D、外电路中每通过0.2mol电子,锌的质量理论上减小6.5g |
下列说法正确的是( )
| A、玻璃钢是一种复合材料,由基体和增强体组成,基体起骨架作用 |
| B、SO2溶于水,其水溶液能导电,说明SO2是电解质 |
| C、食醋、纯碱、食盐分别属于酸、碱、盐 |
| D、生铁、不锈钢、青铜都属于合金 |
下列判断正确的是( )
| A、酸酐一定是氧化物 |
| B、碱性氧化物一定是金属氧化物 |
| C、离子化合物只能在熔化状态下能导电 |
| D、共价化合物一定是非电解质 |