下列物质的电子式书写正确的是 ( )
A、 |
B、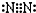 |
C、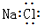 |
D、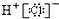 |
下列说法不正确的是( )
| A、使用太阳能热水器、沼气的利用、玉米制乙醇都涉及到生物质能的利用 |
| B、石油、煤、天然气、可燃冰、植物油都属于化石燃料 |
| C、向汽油中添加甲醇后,该混合燃料的热值不变 |
| D、利用太阳能在催化剂参与下分解水制氢是把光能转化为化学能的绿色化学方法 |
下列有关化学用语的表示正确的是( )
| A、HClO的结构式:H-Cl-O |
| B、硝基和二氧化氮两种粒子所含电子数相等 |
C、甲烷分子的比例模型是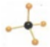 |
D、甲基的电子式: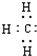 |
低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:2NH3(g)+NO(g)+NO2(g)
2N2(g)+3H2O(g)△H<0,在恒容的密闭容器中,下列有关说法正确的是( )
| 130℃ |
| 催化剂 |
| A、平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
| B、平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小 |
| C、单位时间内消耗NO和N2的物质的量比为1:2时,反应达到平衡 |
| D、其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 |
如果ag某气体中含有的分子数为b,则cg该气体的物质的量为(设阿伏加德罗常数为NA)( )
A、
| ||
B、
| ||
C、
| ||
D、
|
已知反应①:CO(g)+CuO(s)?CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)?Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)?CO2(g)+H2(g)的平衡常数为K.则下列说法正确的是( )
A、反应①的平衡常数K1=
| ||
B、反应③的平衡常数K=
| ||
| C、对于反应③,恒容时,温度升高,H2浓度减小,则该反应为吸热反应 | ||
| D、对于反应③,恒温恒容下,增大压强,H2浓度一定增大 |
按照阿伏加德罗定律,下列叙述不正确的( )
| A、同温同压下两种气体的体积之比等于物质的量之比 |
| B、同温同压下两种气体的物质的量之比等于密度之比 |
| C、同温同压下两种气体的密度之比等于摩尔质量之比 |
| D、同温同体积下两种气体的物质的量之比等于压强之比 |
将1mol SO2和1mol O2通入体积不变的密闭容器中,在一定条件下发生反应2SO2(g)+O2(g)
2SO3(g),达到平衡时SO3 为0.3mol,此时若移走0.5mol O2和0.5mol SO2,相同温度下再次达到新平衡时SO3的物质的量为( )
| 催化剂 |
| △ |
| A、0.3mol |
| B、0.15mol |
| C、小于0.15mol |
| D、大于0.15mol,小于0.3mol |
在一密闭容器中加入一定物质的量的A气体,发生 a A(g)?b B(g)+c C(g)反应,达平衡后,保持温度不变,将容器体积扩大为原来的一倍,当达到新的平衡时c(A)变为原平衡的40%,下列说法正确的是( )
| A、化学计量数之间的关系:a>b+c |
| B、物质B的体积分数减小 |
| C、平衡向正反应方向移动 |
| D、平衡移动过程中,与原平衡相比v正增大、v逆减小 |
将a%的某物质的水溶液加热蒸发掉m g水(溶质不挥发、且蒸发过程无溶质析出),所得溶液体积为V L,溶质的质量分数为蒸发前的2倍,设溶质的相对分子质量为M,则蒸发后所得溶液的物质的量浓度为( )mol/L.
A、
| ||
B、
| ||
C、
| ||
D、
|