有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族; X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料.下列说法中,正确的是( )
| A、X、M两种元素只能形成X2M型化合物 |
| B、元素Y、Z、W的单质晶体属于同种类型的晶体 |
| C、元素W和M的某些单质可作为水处理中的消毒剂 |
| D、由于W、Z、M元素的氢气化物相对分子质量依次减小,所以其沸点依次降低 |
原子序数依次增大的X、Y、Z、W四种短周期元素,X、W原子的最外层电子数与其电子层数相等,X、Z的最外层电子数之和与Y、W的最外层电子数之和相等.甲的化学式为YX3,是一种刺激性气味的气体,乙的化学式为YZ3,丙是由X、Y、Z组成的盐.下列说法正确的是( )
| A、原子半径:W>Y>Z,而离子半径:Z>Y>W |
| B、甲沸点远高于乙,可能是甲分子间存在氢键所致 |
| C、测得丙的水溶液呈酸性,则溶液中丙盐阳离子浓度大于酸根离子浓度 |
| D、W的氯化物水溶液中通入YX3至过量,现象是先有白色沉淀,后逐渐溶解 |
下列说法正确的是( )
| A、△H>0、△S>0的反应一定不能自发进行 |
| B、反应4Al(s)+3O2(g)=2Al2O3 (s)的△H<0、△S>0 |
| C、反应物分子有效碰撞次数增加则反应物的浓度一定增加 |
| D、压强和浓度对反应速率的影响都是通过改变单位体积活化分子数从而影响有效碰撞次数实现的 |
下列说法正确的是( )
A、根据反应Cu+H2SO4
| ||||
| B、电解含Pb(NO3)2和Cu(NO3)2的溶液,阴极上阳离子得电子次顺依次是Cu2+、H+、Pb2+ | ||||
| C、含amolNa2S的溶液最多能吸收2.5amol的二氧化硫气体 | ||||
| D、因Cl2的氧化性强于I2的氧化性,所以置换反应I2+2NaClO3═2NaIO3+Cl2不能发生 |
下列物质熔点比较错误的( )
| A、Na<Mg<Al |
| B、Br2<Cl2<I2 |
| C、硅<碳化硅<金刚石 |
| D、AlCl3<KCl<NaCl |
若某原子的摩尔质量是M g?mol-1,阿伏加德罗常数为NA mol-1,一个12C的质量为m g,则一个该原子的真实质量是( )
A、
| ||
B、
| ||
| C、M?NA g | ||
D、
|
如图所示,△H1=-393.5kJ?mol-1,△H2=-395.4kJ?mol-1,下列说法或表示式正确的是( )
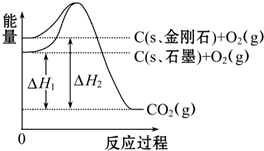

| A、C(s、石墨)═C(s、金刚石)△H=+1.9 kJ?mol-1 |
| B、石墨和金刚石的转化是物理变化 |
| C、金刚石的稳定性强于石墨 |
| D、1 mol石墨的能量比1 mol金刚石的总能量大 |
下列说法或表示方法正确的是( )
| A、等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| B、在稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热大于57.3kJ |
| C、在101kPa时,2g的氢气完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l)△H=-285.8kJ/mol |
| D、由C(s,石墨)=C(s,金刚石)△H=+1.90kJ/mol可知,石墨比金刚石稳定 |
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+49.0kJ/mol ②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g)?△H=-192.9kJ/mol根据上述反应,下列说法正确的是( )
A、 反应①中的能量变化如图所示 |
| B、可推知2H2(g)+O2(g)=2H2O(g)?△H=-483.8 kJ/mol |
| C、1 mol CH3OH充分燃烧放出的热量为192.9 kJ |
| D、CH3OH转变成H2的过程一定要吸收能量 |
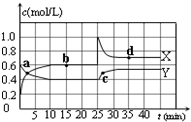 已知:2NO2(g)?N2O4(g);△H<0.在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
已知:2NO2(g)?N2O4(g);△H<0.在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.