已知三种一元弱酸的电离常数大小如下:Ka(HX)>Ka(HY)>Ka(HZ);常温下pH相等的下列三种溶液:NaX、NaY、NaZ,其物质的量浓度从大到小的顺序正确的是( )
| A、c(NaX)>c(NaY)>c(NaZ) |
| B、c(NaZ)>c(NaY)>c(NaZ) |
| C、c(NaX)>c(NaZ)>c(NaY) |
| D、c(NaZ)>c(NaX)>c(NaY) |
在密闭容器中发生下列反应:aA(g)?cC(g)+dD(g),反应达到平衡后,将容积扩大为原来的2倍,当再次达到平衡时,D的浓度为原来平衡的0.3倍,下列叙述正确的是( )
| A、平衡向正反应方向移动 |
| B、a>c+d |
| C、D的体积分数变大 |
| D、A的转化率变大 |
NaHCO3和NaHSO4的溶液混合后,实际参加反应的离子是( )
| A、H+和CO32- |
| B、HCO3-和HSO4- |
| C、Na+、HCO3-和H+ |
| D、HCO3-和H+ |
溴酸银(AgBrO3)溶解度随温度变化曲线如图所示,下列说法错误的是( )
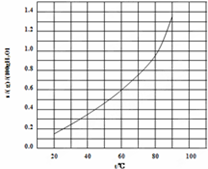

| A、溴酸银的溶解是放热过程 |
| B、温度升高时溴酸银溶解速度加快 |
| C、60℃时溴酸银的KSP约等于6.25×10-4 |
| D、若硝酸钾中含有少量溴酸银,可用重结晶方法提纯 |
在一固定体积的密闭容器中,进行下列反应:CO2(g)+H2(g)?CO(g)+H2O(g)△H=a kJ?mol-1
其化学平衡常数K和温度T的关系如下表所示:则下列有关叙述正确的是( )
其化学平衡常数K和温度T的关系如下表所示:则下列有关叙述正确的是( )
| T(℃) | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
| A、a<0 |
| B、可测量容器总压变化来判定化学反应是否达到平衡 |
| C、温度为830℃时,若c(CO2)?c(H2)>c(CO)?c(H2O),此时v正>v逆 |
| D、温度不变,增大c(CO2),平衡右移,K增大 |
恒温恒容下,当反应容器中总压强不随时间变化时,下列可逆反应不一定达平衡的是( )
| A、2H2(g)+3H2(g)?2NH3(g) |
| B、H2O(g)+C(s)?CO(g)+H2(g) |
| C、H2(g)+I2(g)?2HI(g) |
| D、2NO2(g)?N2O4(g) |
下列各组中,每种电解质溶液电解时只生成氢气和氧气的是( )
| A、NaOH、H2SO4、Ba(OH)2 |
| B、NaOH、CuSO4、H2SO4 |
| C、HCl、CuCl2、Ba(OH)2 |
| D、NaBr、H2SO4、Ba(OH)2 |
 可逆反应:mA(s)+nB(g)?qC(g)在一定温度的密闭容器中进行,B的体积分数(B%)与压强的关系如图所示.下列叙述正确的是( )
可逆反应:mA(s)+nB(g)?qC(g)在一定温度的密闭容器中进行,B的体积分数(B%)与压强的关系如图所示.下列叙述正确的是( )| A、m+n<q |
| B、n>q |
| C、n<q |
| D、x点时,v(正)<v(逆) |