下列有关原子结构和元素周期律表述正确的是( )
| A、原子序数为15的元素的最高化合价为+3 |
| B、第ⅦA族元素是同周期中非金属性最强的元素 |
| C、Li、Na、K、Rb、Cs的得电子能力逐渐增强 |
| D、原子序数为12的元素位于元素周期表的第三周期的ⅡA族 |
在1200℃时,天然气脱硫工艺中会发生下列反应:
H2S(g)+O2(g)═SO2(g)+H2O(g)△H1
2H2S(g)+SO2(g)═S2(g)+2H2O(g)△H2
H2S(g)+O2(g)═S(g)+H2O(g)△H3
2S(g)═S2(g)△H4
则△H4的正确表达式为( )
H2S(g)+O2(g)═SO2(g)+H2O(g)△H1
2H2S(g)+SO2(g)═S2(g)+2H2O(g)△H2
H2S(g)+O2(g)═S(g)+H2O(g)△H3
2S(g)═S2(g)△H4
则△H4的正确表达式为( )
A、△H4=
| ||
B、△H4=
| ||
C、△H4=
| ||
D、△H4=
|
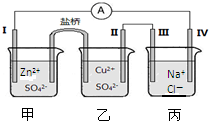 某小组为了探究电化学原理,设计了如图所示的电化学装置,电极Ⅰ为锌,其它电极均为石墨,盐桥是浸泡了饱和氯化钾溶液的琼脂,丙池是滴加了酚酞的氯化钠溶液,下列叙述正确的是( )
某小组为了探究电化学原理,设计了如图所示的电化学装置,电极Ⅰ为锌,其它电极均为石墨,盐桥是浸泡了饱和氯化钾溶液的琼脂,丙池是滴加了酚酞的氯化钠溶液,下列叙述正确的是( )| A、电子由电极Ⅳ通过外电路流向电极Ⅰ |
| B、装置工作过程中Ⅲ电极周围出现红色 |
| C、电极Ⅱ发生还原反应 |
| D、盐桥中Cl-向乙池移动 |
氮氧化物与悬浮在大气中海盐粒子的相互反应:4NO2(g)+2NaCl(s)═2NaNO3(s)+2NO(g)+Cl2(g),△H在恒温条件下,向2L恒容密闭容器中加入0.4mol NO2和0.2mol NaCl,10min反应达到平衡时n(NaNO3)=0.1mol,NO2的转化率为α.下列叙述中正确的是( )
| A、10min内NO浓度变化表示的速率v(NO)=0.01 mol?L-1?min-1 |
| B、若保持其他条件不变,在恒压下进行该反应,则平衡时NO2的转化率大于α |
| C、若升高温度,平衡逆向移动,则该反应的△H>0 |
| D、若起始时向容器中充入NO2(g) 0.1 mol、NO(g)0.2 mol和Cl2(g)0.1 mol(固体物质足量),则反应将向逆反应方向进行 |
对于平衡体系mA(g)+nB(g)?pC(g)+qD(g)△H>0.下列结论中不正确的是( )
| A、若温度不变,将容器的体积缩小到原来的一半,此时A的浓度变为原来的2.1倍,则m+n<p+q | ||
| B、若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n | ||
| C、若m+n=p+q,则往含有a mol气体的平衡体系中再加入amolB,达到新平衡时,气体的总物质的量等于2a | ||
D、若温度不变时将压强增大至原来的2倍,达到新平衡时,总体积一定比原体积的
|
下列实验中,有沉淀产生,且沉淀不会消失的是( )
| A、将氨水逐滴滴入AgNO3溶液中,至过量 |
| B、将二氧化碳通入Ca(OH)2 溶液中,至过量 |
| C、将氯气通入AgNO3溶液中好,至过量 |
| D、将二氧化氮通入Ba(OH)2 溶液中,至过量 |
一定条件下存在反应:H2(g)+I2(g)?2HI(g)△H<0,现有三个相同的1L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1mol H2和1mol I2(g),在Ⅱ中充入2molHI(g),在Ⅲ中充入2mol H2和2mol I2(g),700℃条件下开始反应.达到平衡时,下列说法正确的是( )
| A、容器Ⅰ、Ⅱ中正反应速率相同 |
| B、容器Ⅰ、Ⅲ中反应的平衡常数相同 |
| C、容器Ⅰ中的气体颜色比容器Ⅱ中的气体颜色深 |
| D、容器Ⅰ中H2的转化率与容器Ⅱ中HI的转化率之和等于1 |
某实验小组进行了如下所示的实验,下列说法不正确的是( )


| A、红褐色液体为氢氧化铁胶体 |
| B、加入石灰石是为了促进氯化铁水解 |
| C、产生的气泡是HCl气体 |
| D、产生的气泡是CO2 气体 |