设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A、11.2L氧气所含的原子数为NA |
| B、1.9g的H3O+离子中含有的电子数为11NA |
| C、常温常压下96g NO2与N2O4的混合物含有的氧原子数为2NA |
| D、0.5mol/LH2SO4中的H+数为NA |
在一定温度下,向质量分数为a的某溶液(M)中加入等体积的水,所得溶液的质量分数为0.45a,若溶液(M)的密度为ρ1,水的密度为ρ2,则下列说法正确的是( )
| A、ρ1>ρ2 |
| B、ρ1<ρ2 |
| C、ρ1=ρ2 |
| D、无法确定ρ1和ρ2的大小关系 |
设NA表示阿伏加德罗常数的值,下列叙述中不正确的是( )
| A、1.8 g的NH4+离子中含有的电子数为NA |
| B、常温常压下,11.2 L氧气所含的原子数为NA |
| C、常温常压下,48 g O3和O2的混合物含有的氧原子数为3NA |
| D、2.4 g金属镁变为镁离子时失去的电子数为0.2NA |
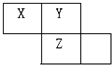 X.Y.Z.W均为短周期元素,它们在元素周期表中的位置如图.若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )
X.Y.Z.W均为短周期元素,它们在元素周期表中的位置如图.若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )| A、Z的氧化物对应的水化物一定是一种强酸 |
| B、原子半径大小顺序是X>Y>Z |
| C、Z单质与Fe反应形成的化合物中,铁元素显+3价 |
| D、Y的单质比Z的单质更易与氢气反应 |
已知aAn+、bB(n+1)+、cCn-、dD(n+1)-均具有相同的电子层结构,下列判断正确的是( )
| A、元素金属性:B>A;元素非金属性:D>C |
| B、原子半径:A>B>C>D |
| C、离子半径:D(n+1)->C n->B (n+1)+>A n+ |
| D、原子序数:b>a>c>d |
将标准状况下的a升氨气溶于1000克水中,得到的氨水的密度为b克/毫升,则该氨水的物质的量的浓度是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列物质中,既含有离子键,又含有共价键的是( )
| A、NaOH |
| B、Na2O |
| C、MgCl2 |
| D、H2O2 |
CH3+、-CH3、CH3-都是重要的有机反应中间体,有关它们的说法正确的是( )
| A、它们互为等电子体,碳原子均采取sp2杂化 |
| B、CH3-与NH3、H3O+互为等电子体,中心原子均为sp3杂化,几何构型均为正四面体形 |
| C、CH3+中的碳原子采取sp2杂化,所有原子均共面 |
| D、CH3+与OH-形成的化合物中含有离子键 |