下列物质的水溶液中,除了水分子外,不存在其它分子的是( )
| A、HF |
| B、HNO3 |
| C、C2H5OH |
| D、新制氯水 |
在下列叙述中,能论证盐酸是强酸,醋酸是弱酸的是( )
| A、将等体积pH=4的盐酸和醋酸稀释到pH=5的溶液,醋酸所加的水量少 |
| B、盐酸和醋酸都可用相应的钠盐和浓硫酸反应制取 |
| C、相同pH的等体积盐酸和醋酸溶液中分别加入相应的钠盐固体,醋酸pH变大,盐酸pH不变 |
| D、相同pH的盐酸和醋酸分别跟锌反应时,产生氢气的起始速率相等 |
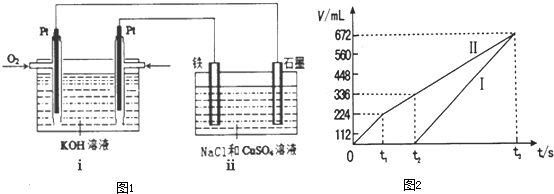
锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环.下列说法正确的是( )


| A、充电时电极b连接电源的正极 |
| B、阳离子交换膜可阻止Br2与Zn直接发生反应 |
| C、放电时正极的电极反应式为Zn-2e-═Zn2+ |
| D、充电时左侧电解质储罐中的离子总浓度增大 |
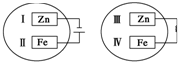 把锌片和铁片放在盛有稀食盐水和K3[Fe(CN)6]试液混合溶液的培养皿中(如图所示平面图),经过一段时间后,下列说法中正确的是( )
把锌片和铁片放在盛有稀食盐水和K3[Fe(CN)6]试液混合溶液的培养皿中(如图所示平面图),经过一段时间后,下列说法中正确的是( )| A、Ⅰ附近溶液pH降低 |
| B、Ⅱ附近很快出现蓝色沉淀 |
| C、Ⅲ附近产生黄绿色气体 |
| D、Ⅳ附近很快生成铁锈 |
已知室温时,0.1mol?L-1某一元酸HA的电离平衡常数约为1×10-7,下列叙述错误的是( )
| A、该溶液的pH=4 |
| B、此溶液中,HA约有0.1%发生电离 |
| C、加水稀释,HA的电离平衡向右移动,HA的电离平衡常数增大 |
| D、由HA电离出的c(H+)约为水电离出的c(H+)的106倍 |
关于如图装置说法正确的是( )
A、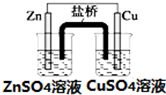 装置中,盐桥中的K+移向ZnSO4溶液 |
B、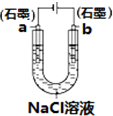 装置工作一段时间后,a极附近溶液的OH-的浓度增大 |
C、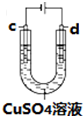 用装置精炼铜时,c极为粗铜 |
D、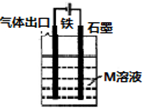 装置中若M是海水,该装置是通过“牺牲阳极保护法”使铁不被腐蚀 |
[双选题]能抑制水的电离,并使溶液中c(H+)>c(OH-)的操作是( )
| A、将水加热煮沸 |
| B、向水中投入一小块金属钠 |
| C、向水中通CO2 |
| D、加入NaHSO4(s) |
下列关于盐酸与醋酸两种稀溶液的说法正确的是( )
| A、相同浓度的两溶液中c(H+)相同 |
| B、100 mL 0.1 mol/L的两溶液分别与氢氧化钠反应至恰好呈中性,盐酸需要的氢氧化钠的物质的量多 |
| C、pH=3的两溶液稀释100倍,醋酸pH变化大 |
| D、两溶液中分别加入少量对应的钠盐固体,c(H+)均明显减小 |