对于重水D2O,在25℃时KW=10-12,定义pD=-lg{c(D+)},pOD=-lg{c(OD-)}.则下列说法正确的是( )
| A、25℃时,纯重水pD=7 |
| B、25℃时,0.1mol/L NaCl的重水溶液pD=pOD=6 |
| C、25℃时,1mol/L的DCl的重水溶液pD=0,pOD=14 |
| D、25℃时,0.01mol/L NaOD的重水溶液中pD=12 |
短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13.X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者是Y原子最外层电子数的3倍.下列说法正确的是( )
| A、X的氢化物溶于水显酸性 |
| B、X与Y形成化合物的化学式为X2Y3 |
| C、Y的氧化物是离子化合物 |
| D、X和Z的最高价氧化物对应的水化物都是弱酸 |
几种短周期元素的原子半径及主要化合价如下表:已知X是短周期中最活泼的金属,且与R同周期.下列叙述不正确的是( )
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6-2 | +5-3 | -2 | +3 |
| A、离子半径大小:R3+<X+<M2- |
| B、Y与M组成的化合物是光化学烟雾的原因之一 |
| C、将YM2通入Ba(NO3)2溶液中有大量白色沉淀产生 |
| D、M氢化物的熔沸点高于Z氢化物的熔沸点 |
已知:①向KMnO4溶液中滴加浓盐酸,产生黄绿色气体; ②向KBr溶液中通入少量实验①产生的气体,溶液变黄色; ③取实验②生成的溶液少量滴在FeCl2与KSCN的混合溶液中,溶液变血红色.根据以上实验,下列判断正确的是( )
| A、上述实验中,共有两个氧化还原反应 |
| B、上述实验证明还原性:Fe2+>Br->Cl->Mn2+ |
| C、实验①生成的气体不能使湿润的淀粉KI试纸变蓝 |
| D、实验③证明Fe2+既有氧化性又有还原性 |
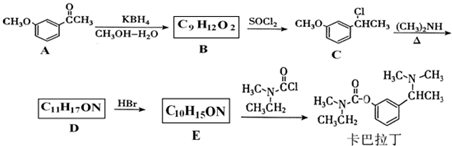
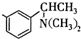 基团 ②属于α-氨基酸 ③含有三个手性碳原子.
基团 ②属于α-氨基酸 ③含有三个手性碳原子.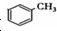 )和丙酮(
)和丙酮(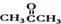 ) 制备化合物
) 制备化合物 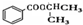 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH
的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH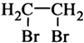
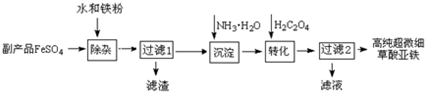
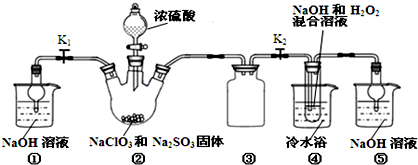
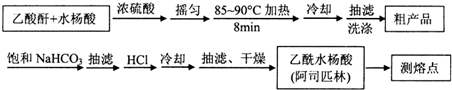
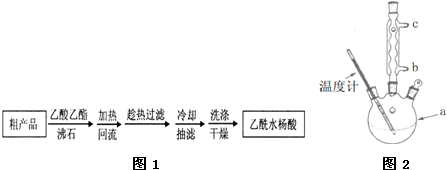
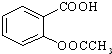 )是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水 S杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水 S杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下: