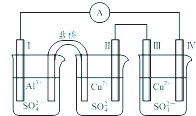
 某同学组装了如图所示的电化学装置,电极Ⅰ为Al电极,其它均为Cu电极,则下列叙述正确的是( )
某同学组装了如图所示的电化学装置,电极Ⅰ为Al电极,其它均为Cu电极,则下列叙述正确的是( )| A、电子流动方向:电极Ⅳ→A→电极Ⅰ |
| B、电极Ⅰ发生氧化反应 |
| C、电极Ⅱ质量不变 |
| D、电极Ⅲ的电极反应:Cu2++2e-=Cu |
下列说法正确的是( )
| A、同一主族的金属元素,从上到下阳离子的氧化性逐渐增强 |
| B、最外层电子数相同的微粒,其化学性质一定相似 |
| C、同周期金属元素的氧化物对应水化物的碱性从左到右依次增强 |
| D、第ⅦA族元素从上到下,其氢化物稳定性减弱而还原性增强 |
下列说法中,正确的是( )
| A、强电解质溶液的导电性比弱电解质溶液的导电性强 |
| B、构成原子核的微粒中都含有中子 |
| C、在原电池中,物质在负极发生氧化反应 |
| D、对于任何反应来说,升高温度、增大压强、加入催化剂都可加快反应速率 |
应用元素周期律分析下列推断,其中正确的是( )
| A、酸性强弱:HClO>H2SO4>H2CO3 |
| B、热稳定性:HF>HCl>HBr |
| C、已知硒(Se)与硫同主族,其最高价氧化物对应的水化物分子式为:H2SeO3 |
| D、原子半径大小:Na>P>N |
下表是3种物质的溶解度(20℃),下列说法中正确的是( )
| 物质 | MgCl2 | Mg(OH)2 | MgCO3 |
| 溶解度(g/100g) | 74 | 0.000 84 | 0.01 |
| A、已知MgCO3的Ksp=6.82×10-6 mol2?L-2,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)?c(CO32-)=6.82×10-6 mol2?L-2 |
| B、除去粗盐中含有的MgCl2杂质,最佳除杂试剂为Na2CO3溶液 |
| C、将表中三种物质与水混合,加热、灼烧,最终的固体产物相同 |
| D、用石灰水处理含有Mg2+和HCO3-的硬水,发生的离子反应方程式为Mg2++2HCO3-+Ca2++2OH-═CaCO3↓+MgCO3↓+2H2O |
Na2O2、CaC2都是离子化合物,都能与水反应放出气体.它们 ( )
| A、阴阳离子个数比均为1:1 |
| B、都含有非极性的共价键 |
| C、与水都发生氧化还原反应 |
| D、放出的都是可燃性气体 |
下列关系与共价键键能无关的是( )
| A、热稳定性:HCl>HBr |
| B、熔沸点:SiO2>SiC |
| C、熔沸点:C12>F2 |
| D、熔沸点:金刚石>单晶硅 |
pH相同、体积相同的氨水和氢氧化钠溶液分别采取下列措施,有关叙述正确的是…( )
| A、加入适量的氯化铵晶体后,两溶液的pH均碱小 |
| B、温度下降10°C,两溶液的pH均不变 |
| C、分别加水稀释10倍,两溶液的pH仍相等 |
| D、用同浓度的盐酸中和,消耗盐酸的体积相同 |