设NA为阿伏加德罗常数的数值,下列说法错误的是( )
| A、一定条件下,2molSO2和1molO2混合在密闭容器中充分反应后容器中的分子数大于2NA |
B、256g S8分子中含S-S键为7NA个  |
| C、由1molCH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-数目为NA个 |
| D、1 mol Na与O2完全反应,生成Na2O和Na2O2的混合物,转移电子总数为NA个 |
用NA表示阿伏加德罗常数的值.下列说法不正确的是( )
| A、0.5molCl2与铁反应转移电子数为NA |
| B、在标准状况下,NA个任何分子所占的体积均约为22.4L |
| C、300mL 5mol/L KNO3溶液与300mL 5mol/L KCl溶液含有的离子数均约为3NA |
| D、16gO2和O3中所含的氧原子数均为NA |
NA表示阿伏加德罗常数,下列判断正确的是( )
| A、常温常压下,16g甲烷分子所含质子数为10NA |
| B、1 mol Cl2参加反应转移电子数一定为2NA |
| C、标准状况下,22.4L乙醇的分子数为NA |
| D、1 L 0.01 mol的Na2CO3溶液中含有0.01NA个CO32- |
在相同条件下,若A容器中的氢气与B容器中的氨气(NH3)所含原子数相等,则两个容器的体积比为( )
| A、1:2 | B、1:3 |
| C、2:3 | D、2:1 |
同温同压下,相同质量的下列气体中体积最大的是( )
| A、N2 |
| B、O2 |
| C、Cl2 |
| D、CO2 |
下列有关化学用语正确的是( )
A、Cl-离子的结构示意图: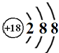 |
B、次氯酸的电子式 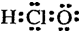 |
C、丙烷分子的比例模型示意图: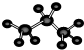 |
D、甲烷的结构式为: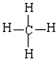 |
有两份铝粉,分别投入盐酸中(甲)和氢氧化钠溶液中(乙),在相同条件下产生氢气的体积相等,则甲、乙反应中转移电子的物质的量之比是( )
| A、1:l | B、1:2 |
| C、1:3 | D、1:4 |
元素性质呈现周期性变化的根本原因是( )
| A、原子半径呈周期性变化 |
| B、元素化合价呈周期性变化 |
| C、电子层数逐渐增加 |
| D、元素原子的核外电子排布呈周期性变化 |
有关物质的性质可以用元素周期律解释的是( )
| A、酸性:HCl>H2S>H2O |
| B、密度:Na>K>Li |
| C、沸点:NH3>AsH3>PH3 |
| D、稳定性:HF>HCl>HBr |