与铁相似,金属锡能与盐酸反应生成氯化亚锡(SnCl2),氯化亚锡又能被氯化铁氧化为氯化锡(SnCl4).则下列有关粒子氧化性和还原性强弱的比较中,正确的是( )
| A、氧化性:Sn4+<Sn2+ |
| B、氧化性:Fe3+<Sn4+ |
| C、还原性:Fe2+<Sn2+ |
| D、还原性:Fe<Sn |
下列有关共价键的说法正确的是( )
| A、分子晶体中共价键越强,熔沸点越高 |
| B、只含共价键的物质,一定是共价化合物 |
| C、两种元素组成的分子中一定只含有极性共价键 |
| D、分子晶体中,可能不存在共价键,但一定存在分子间作用力 |
某一化学反应在不同条件下的能量变化曲线如图所示.下列说法正确的是( )
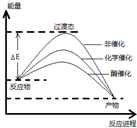

| A、化学催化比酶催化的效果好 |
| B、使用不同催化剂可以改变反应的能耗 |
| C、反应物的总能量低于生成物的总能量 |
| D、使用不同催化剂可以改变反应的热效应 |
NH5属于离子晶体.与水反应的化学方程式为:NH5+H2O→NH3?H2O+H2↑,它也能跟乙醇发生类似的反应,并都产生氢气.有关NH5叙述正确的是( )
| A、与乙醇反应时,NH5被氧化 |
| B、NH5中N元素的化合价为+5价 |
| C、1 mol NH5中含有5 molN-H键 |
| D、1 mol NH5与H2O完全反应,转移电子2 mol |
工业上用CO和H2合成CH3OH:CO(g)+2H2(g)?CH3OH(g).反应的平衡常数如下表:
下列说法正确的是( )
| 温度/℃ | 0 | 100 | 200 | 300 | 400 |
| 平衡常数 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
| A、该反应的△H>0 |
| B、加压、增大H2浓度和加入催化剂都能提高CO的转化率 |
| C、工业上采用5×103kPa和250℃的条件,其原因是原料气的转化率高 |
| D、t℃时,向1 L密闭容器中投入0.1 mol CO和0.2 mol H2,平衡时CO转化率为50%,则该温度时反应的平衡常数的数值为100 |
工业上常用氯氧化法处理含氰(CN-)废水,一定条件下,氯气和CN-反应生成无毒气体.下列说法不正确的是( )
| A、CN-中碳元素的化合价为+2 |
| B、该反应的产物之一是无毒的N2 |
| C、当1 mol CN-参与反应时,转移3 mol e- |
| D、处理含0.1 mol CN-的废水,理论上需要消耗标准状况下Cl2的体积为5.6 L |
关于下列装置的说法正确的是( )
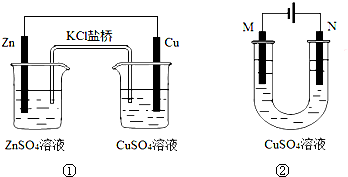

| A、装置①中盐桥内的K+移向CuSO4溶液 |
| B、装置①将电能转变为化学能 |
| C、若装置②用于铁棒镀铜,则N极为铁棒 |
| D、若装置②用于电解精炼铜,溶液中的Cu2+浓度保持不变 |
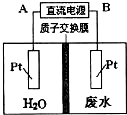 用如图所示装置处理含NO3-的酸性工业废水,某电极反应式为2NO3-+12H++10e-=N2+6H2O,则下列说法错误的( )
用如图所示装置处理含NO3-的酸性工业废水,某电极反应式为2NO3-+12H++10e-=N2+6H2O,则下列说法错误的( )| A、电源正极为A,电解过程中有气体放出 |
| B、电解时H+从质子交换膜左侧向右侧移动 |
| C、电解过程中,右侧电解液pH保持不变 |
| D、电解池一侧生成5.6g N2,另一侧溶液质量减少l8g |
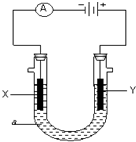 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.