关于图中各装置的叙述不正确的是( )


| A、装置①是中和滴定法测定硫酸的物质的量浓度 |
| B、装置②中手捂烧瓶(橡胶管已被弹簧夹夹紧),发现导管中有液柱上升并保持稳定,则说明装置不漏气 |
| C、装置③中X若为四氯化碳,可用于吸收氨气,并防止倒吸 |
| D、装置④证明铁生锈过程中空气参与反应 |
室温下,下列有关两种溶液的说法不正确的是( )
| 序号 | ① | ② |
| pH | 12 | 12 |
| 溶液 | 氨水 | 氢氧化钠溶液 |
| A、①②两溶液中c(OH-)相等 |
| B、①溶液的物质的量浓度为0.01 mol?L-1 |
| C、①②两溶液分别加水稀释10倍,稀释后溶液的pH:①>② |
| D、等体积的①②两溶液分别与0.01 mol?L-1的盐酸完全中和,消耗盐酸的体积:①>② |
室温时,0.01mol?L-1HA溶液的pH=3,向该溶液中逐滴加入NaOH,在滴加过程中,下列有关叙述正确的是( )
| A、原HA溶液中,c(H+)=c(OH-)+c(A-) |
| B、当恰好完全中和时,溶液呈中性 |
| C、当滴入少量的NaOH,促进了HA的电离,溶液的pH升高 |
| D、当NaOH溶液过量时,可能出现:c(A-)>c(Na+)>c(OH-)>c(H+) |
25℃时将10mLpH=11的氨水加水稀释至100mL,下列判断正确的是( )
| A、稀释后溶液的pH=7 | ||||
| B、氨水的电离度增大,溶液中所有离子的浓度均减小 | ||||
C、稀释过程中
| ||||
| D、pH=11氨水的浓度为0.001mol/L |
如图所示对实验Ⅰ~Ⅳ的实验现象预测正确的是( )
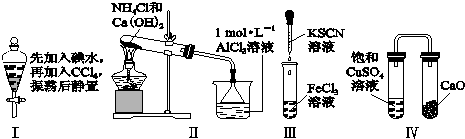

| A、实验Ⅰ:液体分层,下层呈无色 |
| B、实验Ⅱ:烧杯中先出现白色沉淀,后溶解 |
| C、实验Ⅲ:试管中立刻出现红色沉淀 |
| D、实验Ⅳ:放置一段时间后,饱和CuSO4溶液中出现蓝色晶体 |
已知酸性: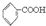 >H2CO3>
>H2CO3> >HCO3-将
>HCO3-将 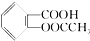 转变为
转变为 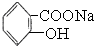 ,可行的方法是( )
,可行的方法是( )
 >H2CO3>
>H2CO3> >HCO3-将
>HCO3-将  转变为
转变为  ,可行的方法是( )
,可行的方法是( )| A、向该溶液中加入足量的稀硫酸,加热 |
| B、将该物质与稀硫酸共热后,再加入足量的NaOH溶液 |
| C、将该物质与足量的NaOH溶液共热,再通入足量CO2气体 |
| D、将该物质与稀硫酸共热后,再加入足量的NaHCO3溶液 |
下列实验能达到实验目的是( )
| A、检验NH4+时,往试样中加入NaOH溶液,微热,用湿润的蓝色石蕊试纸检验逸出的气体 |
| B、向做完蔗糖水解后的溶液中直接加入新制的Cu(OH)2并加热,以检验蔗糖是否水解 |
| C、将混有HCl的CO2通入饱和Na2CO3溶液中除去HCl |
| D、将Al2(SO4)3溶液蒸干制备Al2(SO4)3固体 |
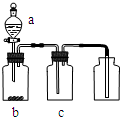 用如图装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是( )
用如图装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是( )