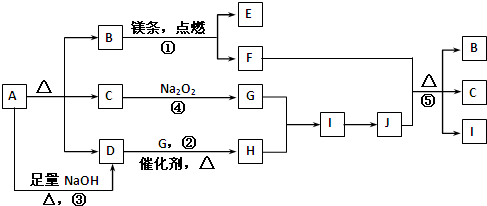
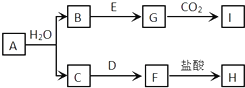
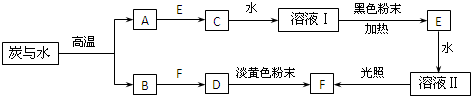
下列离子方程式正确的是( )
| A、NH4HCO3溶液中加入少量稀NaOH溶液:NH4++OH-=NH3?H2O |
| B、FeBr2溶液中通入足量的氯气:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
| C、硫酸亚铁溶液中加入用硫酸酸化的双氧水Fe2++2H++H2O2=Fe3++2H2O |
| D、在通入过量SO2后的NaOH溶液中加足量的溴水(不考虑SO2的溶解):HSO3-+Br2+H2O=3H++2Br-+SO42- |
下列离子方程式表达正确的是( )
| A、漂白粉溶液中通入过量的CO2:ClO-+CO2+H2O=HClO+HCO3- | ||||
| B、用碳酸钠溶液吸收Br2:CO32-+Br2+2H2O=Br-+BrO3-+CO2↑+4H+ | ||||
C、用铜电极电解硫酸铜溶液:2Cu2++2H2O
| ||||
| D、已知硫酸铅难溶于水,也难溶于硝酸,却可溶于醋酸铵溶液中,形成无色溶液,当在Pb(Ac)2醋酸铅溶液中通入H2S时,有黑色沉淀PbS生成:Pb2++2Ac-+H2S=PbS+2HAc |
X、Y、Z、W为原子序数依次增大的短周期元素.其形成的小分子化合物Y2X2、Z2X4、X2W2中,分子内各原子最外层电子都满足稳定结构.下列说法正确的是( )
| A、X、Y、Z、W的原子半径的大小关系为:W>Y>Z>X |
| B、在Y2X2、Z2X4、X2W2的一个分子中,所含的共用电子对数相等 |
| C、X、Y、Z、W四种元素可形成化学式为X7Y2ZW2的化合物 |
| D、与元素Y、Z相比,元素W形成的简单氢化物最稳定,是因为其分子间存在氢键 |
已知A、B、C、D四种物质中均含同种元素,且它们之间的转化关系如图.下列说法正确的是( )
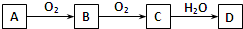
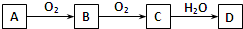
| A、A一定为单质 |
| B、C一定为氧化物 |
| C、D一定为酸 |
| D、A、B、C的相对分子质量之差为16或16的倍数 |
铁铜合金中逐滴加入稀硝酸的过程中,下列离子方程式较难发生的是( )
| A、Fe+4H++NO3-→Fe3++NO↑+2H2O |
| B、3Fe+8H++2 NO3-→3Fe2++2NO↑+4H2O |
| C、3Cu+8H++2 NO3-→3Cu2++2NO↑+4H2O |
| D、3Fe2++4H++NO3-→3Fe3++NO↑+2H2O |
X、Y、Z、W四种短周期元素的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族.下列叙述正确的是( )
| A、元素X只能形成一种氢化物:H2X |
| B、元素W的最高价氧化物对应水化物的酸性比Z的弱 |
| C、原子半径的大小顺序:r(Y)>r(Z)>r(W)>r(X) |
| D、化合物YX、ZX2、WX3中化学键的类型相同 |