下列关于物质的量的叙述中,正确的是( )
| A、1mol食盐含有6.02×1023个分子 |
| B、Mg的摩尔质量为24 |
| C、1mol水中含有2mol氢和1mol氧 |
| D、1molNe含有6.02×1024个电子 |
对于Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g)△H=?的化学反应,下列叙述不正确的是( )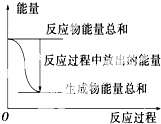

| A、反应过程中能量关系如上图表示,则该反应为放热反应 |
| B、若将其设计为原电池,当有32.5 g锌溶解时,正极放出气体一定为11.2 L |
| C、化学反应的焓变与反应方程式的计量数有关 |
| D、若将该反应设计成原电池,锌为负极 |
物质发生化学反应时,下列量值在反应前后肯定不发生变化的是( )
①电子总数; ②原子总数; ③分子总数; ④物质的种类;⑤物质的总质量;⑥物质所具有的总能量.
①电子总数; ②原子总数; ③分子总数; ④物质的种类;⑤物质的总质量;⑥物质所具有的总能量.
| A、①②⑤ | B、②⑤⑥ |
| C、①②③⑤ | D、①②⑤⑥ |
取100mL 0.3mol?L-1和300mL 0.25mol?L-1的硫酸注入500mL容量瓶中,加水稀释至刻度线,该混合溶液中硫酸的物质的量浓度是( )
| A、0.21mol?L-1 |
| B、0.42mol?L-1 |
| C、0.56mol?L-1 |
| D、0.26mol?L-1 |
下列有关说法正确的是( )
| A、在101 kPa时,1molCH4完全燃烧生成CO2和水蒸气放出的热量就是CH4的燃烧热 |
| B、除去苯中混有的苯酚,可滴加浓溴水,再经过滤除去 |
C、已知:C-C、C=C、C-H、H-H键能分别为348,610,413,436(单位均为kJ/mol)则可以计算出反应 的△H为-384 kJ/mol 的△H为-384 kJ/mol |
| D、含1mol NaOH的稀溶液分别和含1mol CH3COOH、1molHNO3的稀溶液反应,前者比后者放出的热量少 |
电化学降解NO3-的原理如图所示.下列说法中不正确的是( )


| A、铅蓄电池的A极为正极,电极材料为PbO2 |
| B、铅蓄电池工作过程中负极质量增加 |
| C、该电解池的阴极反应为:2NO3-+6H2O+10e-=N2↑+12OH- |
| D、若电解过程中转移2moL电子,则交换膜两侧电解液的质量变化差(△m左-△m右)为10.4g |
已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd+2NiOOH+2H2O
Cd(OH)2+2Ni(OH)2有关其说法正确的是( )
| 充电 |
| 放电 |
| A、充电过程是化学能转化为电能的过程 |
| B、放电时负极附近溶液的碱性不变 |
| C、放电时电解质溶液中的OH-向正极移动 |
| D、充电时阳极反应:Ni(OH)2-e-+OH-=NiOOH+H2O |
以下现象与电化学腐蚀有关的是( )
| A、炒菜的铁锅容易生锈 |
| B、生铁比纯铁容易生锈 |
| C、运输石油的管道表面变暗 |
| D、银质奖牌(纯银制成)久置后表面变暗 |
下列有关说法正确的是( )
| A、镀锌铁制品镀层受损后,铁制品比受损前更容易生锈 |
| B、2NaHCO3(s)=Na2CO3(s)+CO2(g)+H2O(l)室温下不能自发进行,说明该反应的△H<0 |
| C、加热0.1 mol?L-1CH3COONa 溶液,CH3COO-的水解程度和溶液的pH均增大 |
| D、N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变时升高温度,反应速率v(H2 )和H2的平衡转化率均增大 |
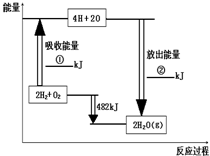 已知拆开1mol氢气中的化学键需要消耗436kJ能量,拆开1mol氧气中的化学键需要消耗498kJ能量,根据如图中的能量图,回答下列问题:
已知拆开1mol氢气中的化学键需要消耗436kJ能量,拆开1mol氧气中的化学键需要消耗498kJ能量,根据如图中的能量图,回答下列问题: