某化学反应的能量变化如图所示.下列有关叙述正确的是( )


| A、该反应为放热反应 |
| B、E2可表示形成新的化学键所释放的能量 |
| C、该反应的反应热△H=E1-E2 |
| D、加入催化剂可同等程度的降低E1、E2 |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、在常温、常压下,11.2 L N2含有的分子数为0.5 NA |
| B、标准状况下,22.4 L H2和O2的混合物所含分子数为NA |
| C、标准状况下,18 g H2O的体积是22.4 L |
| D、1 mol SO2的体积是22.4 L |
下列说法正确的是( )
| A、烧碱固体在水中溶解的过程是放热反应 |
| B、P2O5和CaO可以作干燥剂,利用了它们具有易潮解的性质 |
| C、FeCl3固体溶于蒸馏水可制得FeCl3溶液 |
| D、粗盐易潮解是因为其中含有CaCl2和MgCl2等杂质的缘故 |
下列有关概念的说法正确的是( )
| A、燃烧热只针对可燃物和氧气反应而言 |
| B、中和热只针对强酸与强碱反应而言 |
| C、溶解平衡只针对难溶物而言 |
| D、电解池只针对自发进行的氧化还原反应而言 |
设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A、16g O3与 O2混合物中所含氧原子数为NA |
| B、2.3gNa+中含有的电子数为0.1NA |
| C、在常温常压下11.2L二氧化碳所含的分子数目为0.5NA |
| D、相同质量的两块钠分别变成氧化钠和过氧化钠前者失去的电子数多 |
下列条件下,两瓶气体所含原子数一定相等的是( )
| A、同压强、同温度的O2和O3 |
| B、同温度、同体积的NH3和N2 |
| C、同体积、同密度的C2H4和C3H6 |
| D、同压强、同体积的N2O和CO2 |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、10 g NH3含有4NA个电子 |
| B、2 L 0.5 mol?L-1硫酸钾溶液中阴离子所带电荷数为NA |
| C、标准状况下,22.4 L氨水含有NA个NH3分子 |
| D、0.1mol铁和0.1mol铜分别与0.1 mol氯气完全反应,转移的电子数均为0.2NA |
航天飞船可用肼(N2H4)和过氧化氢(H2O2)为动力源.已知1g液态肼和足量液态过氧化氢反应生成氮气和水蒸气时放出20.05kJ的热量.下列说法中错误的是( )
| A、该反应中肼作还原剂 |
| B、液态肼的标准燃烧热为641.6 kJ?mol-1 |
| C、该动力源的突出优点之一是生成物对环境无污染 |
| D、肼和过氧化氢反应的热化学方程式为N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.6 kJ?mol-1 |
下列叙述正确的是( )
| A、乙醇的结构简式为:C2H6O |
B、硫离子的结构示意图为: |
| C、NaHCO3电离:NaHCO3=Na++H++CO32- |
D、氮分子的结构式为: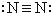 |
用NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A、0.5 mol锌粒与足量盐酸反应产生11.2 L H2 |
| B、标准状况下,11.2 L CCl4所含分子数为0.5NA |
| C、0.1 mol CH4所含氢原子数为0.4NA |
| D、常温常压下,28 g N2中所含原子个数为NA |