NA表示阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,22.4L的CCl4中含有的CCl4分子数为NA |
| B、10mL pH=6的纯水中含有OH-离子数为10-10 NA |
| C、100 mL 1 mol?L-1 的Na2CO3溶液中含有CO32-离子数为0.1NA |
| D、14g由N2与CO组成的混合气体含有的原子数目为NA |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、在反应KIO3+6 HI=KI+3I2+3 H2O中,每生成3mo1 I2转移的电子数为5NA |
| B、室温下,28.0g乙烯和丁烯的混合气体中含有的碳原子数目为3NA |
| C、在1L0.1mol?L-1碳酸钠溶液中,阴离子总数小于0.1NA |
| D、1mol Na2O2 固体中含离子总数为4 NA |
下列仪器的主要成分不属于硅酸盐材料的是( )
①冷凝管 ②明成化斗彩鸡缸杯 ③石英玻璃 ④计算机芯片 ⑤光导纤维.
①冷凝管 ②明成化斗彩鸡缸杯 ③石英玻璃 ④计算机芯片 ⑤光导纤维.
| A、③④⑤ | B、②④⑤ |
| C、①③⑤ | D、②③④ |
NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、25℃时,pH=2的1.0L H2SO4溶液中含有的H+数目为0.02NA |
| B、电解精炼铜时,当电路中转移NA个电子,阳极溶解32g铜 |
| C、2.24LNH3中含共价键数目一定为0.3NA |
| D、向含有FeI2的溶液中通入适量氯气,当有1mol Fe2+被氧化时该反应转移电子的数目至少为3NA |
下列叙述正确的是( )
| A、标准状况下,11.2 L NH3溶于1 L水,溶液中含有N原子的微粒总数为0.6NA |
| B、1.00 mol NaCl中,所有Na+的最外层电子总数约为8×6.02×1023 |
| C、欲配制1.00 L 1.00 mol?L-1的NaCl溶液,可将58.5 g NaCl溶于1.00 L水中 |
| D、1mol FeCl3完全转化为Fe(OH)3胶体后形成NA个胶粒 |
下列化学用语正确的是( )
A、
 | ||
B、某有机物的分子的简易球棍模型如图,分子式为C3H7O2N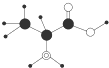 | ||
C、羟基乙酸(HOCH2COOH)的缩聚物: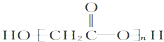 | ||
| D、铁在元素周期表中位于第4周期第ⅧB 族 |
同温同压下,体积相同的两个容器,一个充满NO,另外一个充满N2和O2的混合气体,这两个容器中一定相同的是( )
| A、电子总数 | B、质子总数 |
| C、分子总数 | D、氮原子总数 |
设NA为阿伏加德罗常数,下列说法中,正确的是( )
| A、2.4 g金属镁所含电子数目为0.2 NA |
| B、16 g CH4所含原子数目为NA |
| C、17 g NH3 所含氢原子数目为4 NA |
| D、18 g水所含分子数目为NA |
下列叙述正确的是(用NA代表阿伏加德罗常数的值)( )
| A、金属镁变为镁离子时失去的电子数为2NA |
| B、1molHCl气体中的粒子数与0.5 mo1/L盐酸中溶质粒子数相等 |
| C、在标准状况下,22.4LCH4与18gH2O所含有的电子数均为10 NA |
| D、CO和N2为等电子体,22.4L的CO气体与lmol N2所含的电子数相等 |
下列有关化学用语表示正确的是( )
| A、葡萄糖的结构简式:C6H12O6 | ||
| B、NaHCO3的电离:NaHCO3=Na++H++CO32- | ||
C、质子数为53、中子数为78的碘原子:
| ||
D、CO2的电子式: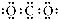 |