已知:①2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol②H2(g)+S(g)=H2S(g)△H=-20.1kJ/mol
下列判断一定正确的是( )
下列判断一定正确的是( )
| A、由①知:氢气的燃烧热△H=-241.8 kJ/mol |
| B、由①、②知:2H2S(g)+O2(g)=2S(g)+2H2O(g)△H=-443.4 kJ/mol |
C、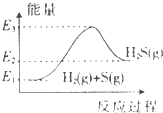 反应②中的能量变化能用图表示 |
| D、若反应②中改用固态硫,放热将大于20.1kJ |
今有如下三个热化学方程式:下列关于它们的叙述正确的是( )
(1)H2(g)+
O2(g)═H2O(g)△H1=a kJ?mol-1;
(2)H2(g)+
O2(g)═H2O(l)△H2=b kJ?mol-1;
(3)2H2(g)+O2(g)═H2O(l)△H3=c kJ?mol-1.
(1)H2(g)+
| 1 |
| 2 |
(2)H2(g)+
| 1 |
| 2 |
(3)2H2(g)+O2(g)═H2O(l)△H3=c kJ?mol-1.
| A、它们都是吸热反应 |
| B、a,b和c均为负值 |
| C、a=b |
| D、2b=c>0 |
下列关于反应热的说法正确的是( )
| A、当△H为负值时,表示该反应为吸热反应 |
| B、燃烧不一定是放热反应 |
| C、反应热的大小与反应物所具有的能量和生成物具有的能量无关 |
| D、反应热的大小只与反应体系的始态和终态有关 |
下列燃烧反应的反应热不是燃烧热的是( )
①H2(g)+
O2(g)═H2O(l)△H1
②C(s)+
O2(g)═CO(g)△H2
③S(s)+O2(g)═SO2(g)△H3
④2H2S(g)+3O2(g)═2SO2(s)+2H2O(l)△H4.
①H2(g)+
| 1 |
| 2 |
②C(s)+
| 1 |
| 2 |
③S(s)+O2(g)═SO2(g)△H3
④2H2S(g)+3O2(g)═2SO2(s)+2H2O(l)△H4.
| A、①③ | B、②④ | C、②③ | D、①④ |
下列事实不能用电化学理论解释的是( )
| A、轮船水线以下的船壳上装一定数量的锌块 |
| B、镀锌的铁比镀锡的铁耐用 |
| C、纯锌与稀硫酸反应时,滴入少量硫酸铜溶液后速率加快 |
| D、铝片不用特殊方法保存 |
有关铜-锌-稀硫酸构成的原电池中的一些说法正确的是( )
| A、锌片为正极,且锌片逐渐溶解 |
| B、铜片为负极,且铜片上有气泡 |
| C、溶液中的H+移向铜极 |
| D、该电池工作的过程中溶液的pH始终不变 |
如图甲是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如图乙所示,则卡片上的描述合理的是( )


| A、①②③ | B、②④ |
| C、④⑤⑥ | D、③④⑤ |
火法炼铜得到的粗铜中含多种杂质(如锌、金和银等),其性能远不能达到电气工业的要求,工业上常使用电解精炼法将粗铜提纯.在电解精炼时( )
| A、粗铜接电源负极 |
| B、纯铜作阳极 |
| C、杂质都将以单质形式沉积到池底 |
| D、纯铜片增重2.56g,电路中通过电子为0.08mol |