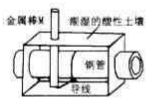
 全世界短年钢铁因锈蚀造成大量的损失.某城市拟用如图所示方法保护埋在酸性土壤中的钢质管道,使其免受腐蚀.关于此方法,下列说法不正确的是( )
全世界短年钢铁因锈蚀造成大量的损失.某城市拟用如图所示方法保护埋在酸性土壤中的钢质管道,使其免受腐蚀.关于此方法,下列说法不正确的是( )| A、土壤中的钢铁易被腐蚀是因为在潮湿的土壤中形成了原电池 |
| B、金属棒X的材料应该是比镁活泼的金属 |
| C、金属棒X上发生反应:M-ne---Mn+ |
| D、这种方法称为牺牲阳极的阴极保护法 |
 A、B、C三个电解槽,如下图所示(其中电极的大小、形状、间距均相同).B、C中溶液浓度和体积相同,通电一段时间后,当A中铜电极的质量增加0.128g时,B中电极上银的质量增加( )
A、B、C三个电解槽,如下图所示(其中电极的大小、形状、间距均相同).B、C中溶液浓度和体积相同,通电一段时间后,当A中铜电极的质量增加0.128g时,B中电极上银的质量增加( )| A、0.054g |
| B、0.108g |
| C、0.216 |
| D、0.432g |
 微型纽扣电池在现代生活中有广泛应用.有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为Zn+2OH--2e-═ZnO+H2O,Ag2O+H2O+2e-═2Ag+2OH-.下列叙述正确的是( )
微型纽扣电池在现代生活中有广泛应用.有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为Zn+2OH--2e-═ZnO+H2O,Ag2O+H2O+2e-═2Ag+2OH-.下列叙述正确的是( )| A、在使用过程中,电解质KOH被不断消耗 |
| B、使用过程中,电子由Ag2O极经外电路流向Zn极 |
| C、每转移2mol e-,有232gAg2O被氧化 |
| D、Zn是负极,Ag2O是正极 |
氮氧化铝(AlON)是一种高硬度防弹材料,可以在高温下由反应Al2O3+C+N2=2AlON+CO合成,下列有关说法正确的是( )
| A、氮氧化铝中氮的化合价是-3 |
| B、反应中每生成5.7g AlON 同时生成1.12 L CO |
| C、反应中氧化产物和还原产物的物质的量之比是2:1 |
| D、反应中氮气作氧化剂 |
已知某条件下,合成氨反应的数据如下:N2(g)+3H2(g)?2ΝΗ3(γ)
当用氨气浓度的增加来表示该反应的速率时,下列说法中错误的是( )
| 起始浓度/mol?L-1 | 1.0 | 3.0 | 0.2 |
| 2s末浓度/mol?L-1 | 0.6 | 1.8 | 1.0 |
| 4s末浓度/mol?L-1 | 0.4 | 1.2 | 1.4 |
| A、2s末氨气的反应速率=0.4mol?(L?s)-1 |
| B、前2s时间内氨气的平均反应速率=0.4mol?(L?s)-1 |
| C、前4s时间内氨气的平均反应速率=0.3mol?(L?s)-1 |
| D、2~4s时间内氨气的平均反应速率=0.2mol?(L?s)-1 |
下列各项叙述中,正确的是( )
| A、钠原子由1s22s22p63s1→1s22s22p63p1时,原子释放能量,由基态转化成激发态 |
| B、2p和3p轨道形状均为哑铃形,能量也相等 |
C、氮原子的价电子排布图: |
| D、价电子排布为4s24p3的元素位于第四周期第ⅤA族,是p区元素] |
气态中性基态原子的原子核外电子排布发生如下变化,吸收能量最多的是( )
| A、1s22s22p63s23p2→1s22s22p63s23p1 |
| B、1s22s22p63s23p3→1s22s22p63s23p2 |
| C、1s22s22p63s23p4→1s22s22p63s23p3 |
| D、1s22s22p63s23p1→1s22s22p63s2 |
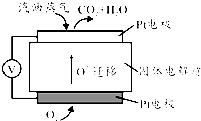
 用气体传感器可以检测汽车尾气中CO的含量.传感器是以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.下列说法正确的是( )
用气体传感器可以检测汽车尾气中CO的含量.传感器是以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.下列说法正确的是( )| A、燃料电池工作时,电极b作负极 |
| B、工作时,电流由负极通过传感器流向正极 |
| C、b电极的电极反应式为:O2+2H2O+4e-═4OH- |
| D、当消耗11.2L(标准状况下)CO时,理论上传感器中会通过NA个电子 |