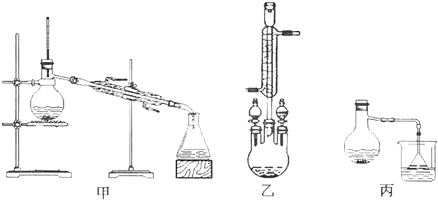
化学中通常用图象直观地描述化学反应进程或结果.下列图象及描述正确的是( )
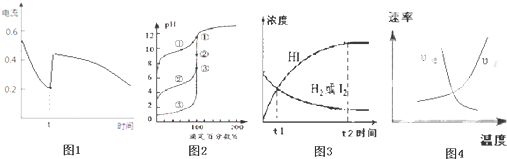

| A、图1表示Zn-Cu原电池反应过程中的电流强度的变化,t时可能加入了双氧水 |
| B、图2表示用0.1000mol?L-1NaOH溶液滴定浓度相同的三种一元酸,曲线①的酸性最强 |
| C、图3表示可逆反应:H2(g)+I2(g)?2HI(g)在一段时间内,各组分浓度的变化图,t1时刻速率关系为:υ正=υ逆 |
| D、图4表示可逆反应:N2(g)+O2(g)?2NO(g)△H<0,正、逆反应速率随温度变化的曲线图 |
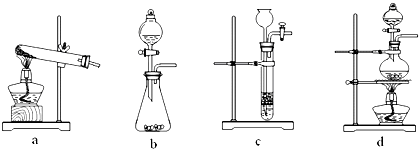
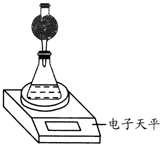 某探究小组用测量HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素.限选试剂:1.00mol?L-1 HNO3、2.00mol?L-1HNO3,细颗粒大理石、粗颗粒大理石,35℃水浴.
某探究小组用测量HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素.限选试剂:1.00mol?L-1 HNO3、2.00mol?L-1HNO3,细颗粒大理石、粗颗粒大理石,35℃水浴. 某实验中,用0.1000mol?L-1标准盐酸测定某NaOH溶液的浓度,其操作步骤如下:
某实验中,用0.1000mol?L-1标准盐酸测定某NaOH溶液的浓度,其操作步骤如下: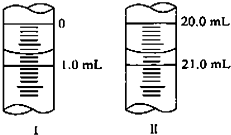 在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:2MnO
在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:2MnO