在3S+6KOH═2K2S+K2SO3+3H2O的反应中,被还原的硫比被氧化的硫多3.2g,则参加反应硫的物质的量为( )
| A、0.1mol |
| B、0.2mol |
| C、0.3mol |
| D、0.4mol |
 可逆反应mA(s)+nB(g)?eC(g)+fD(g)反应过程中,当其他条件不变时,升高温度混合气体密度增大;C的体积分数φ(C)不同压强(P)的条件下随时间(t)的变化关系如图所示.下列叙述错误的是( )
可逆反应mA(s)+nB(g)?eC(g)+fD(g)反应过程中,当其他条件不变时,升高温度混合气体密度增大;C的体积分数φ(C)不同压强(P)的条件下随时间(t)的变化关系如图所示.下列叙述错误的是( )| A、该反应的△H>0 |
| B、化学方程式中,m+n>e+f |
| C、达到平衡后,增加A的质量有利于化学平衡向正反应方向移动 |
| D、达到平衡后,升高温度混合气体平均摩尔质量增大 |
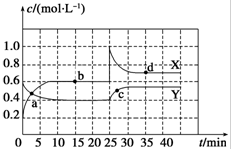 已知NO2和N2O4可以相互转化:N2O4(g)?2NO2(g);△H>0,现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如图.下列说法正确的是( )
已知NO2和N2O4可以相互转化:N2O4(g)?2NO2(g);△H>0,现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如图.下列说法正确的是( )| A、10min前反应向△H<0的方向进行 |
| B、曲线X表示N2O4浓度随时间的变化 |
| C、第二次达到平衡时,平衡常数的值大于0.9 |
| D、反应进行至25min时,曲线发生变化的原因是加入0.4molNO2 |
 在一定温度下的可逆反应:mA(g)+nB(g)?pC(g)+qD(g),生成物C的体积分数与压强p1和p2、时间t1和t2的关系如图所示,则在下列关系式中正确的是( )
在一定温度下的可逆反应:mA(g)+nB(g)?pC(g)+qD(g),生成物C的体积分数与压强p1和p2、时间t1和t2的关系如图所示,则在下列关系式中正确的是( )| A、p1>p2 |
| B、p1<p2 |
| C、m+n>p+q |
| D、m+n=p+q |
关于下列四个图象的说法正确的是( )


| A、已知图①是体系Fe3+(aq)+SCN-(aq)?Fe(SCN)2+(aq)中的c[Fe(SCN)2+]与温度T的平衡图象.A点与B点相比,A点的c(Fe3+)大 |
| B、图②表示镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积V与时间t的关系.则反应中镁和铝的反应速率之比为2:3 |
| C、图③表示电源X极为正极,U形管中为AgNO3溶液,则b管中电极反应式:2H++2e-=H2↑ |
| D、图④是某温度下,相同体积,相同PH的盐酸和醋酸溶液分别加水稀释,pH随溶液 体积V变化的曲线.II为醋酸稀释时PH的变化曲线 |
将4mol A气体和2mol B气体在2L的容器中混合并在一定条件下发生反应:2A(g)+B(g)?2C(g),经2s后测得C的浓度为0.6mol?L-1,下列几种说法中正确的是( )
| A、用物质A表示反应的平均速率为0.3 mol?L-1?s-1 |
| B、用物质B表示反应的平均速率为0.3 mol?L-1?s-1 |
| C、2 s时物质A的转化率为70% |
| D、2 s时物质B的浓度为0.3 mol?L-1 |
关于pH相同的醋酸和盐酸溶液,下列叙述中正确的是( )
| A、相同体积的酸中和氢氧化钠的量相同 |
| B、相同体积的酸分别稀释成相同PH溶液,所加水的量相同 |
| C、相同体积的酸与足量锌粒反应产生氢气的量相同 |
| D、两种酸溶液中阴离子总浓度相同 |

