将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中,下列分析正确的是( )


| A、K1闭合,K2断开,铁棒上发生的反应为2H2O+O2+4e-=4OH- |
| B、K2闭合,K1断开,电路中通过0.002 NA个电子时,两极共产生0.001 mol气体 |
| C、K2闭合,K1断开,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法 |
| D、K1闭合,K2断开,石墨棒周围溶液pH逐渐升高 |
下列各装置能构成原电池的是( )
A、 |
B、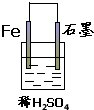 |
C、 |
D、 |
有关下列四个常用电化学装置的叙述中,正确的是( )
 |  | 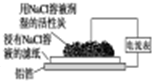 |  |
| 图Ⅰ碱性 锌锰电池 | 图Ⅱ铅硫 酸蓄电池 | 图Ⅲ铝箔的腐蚀 | 图Ⅳ银锌 纽扣电池 |
| A、图Ⅰ所示电池中,MnO2的作用是催化剂,负极反应为:Zn-2e-=Zn2+ |
| B、图Ⅱ所示电池充电过程中,硫酸浓度不断增大,阴极反应为:Pb+SO42-=PbSO4-2e- |
| C、铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl-由活性炭区向铝箔表面区迁移,并发生电极反应:2Cl--2e-═Cl2↑ |
| D、图Ⅳ所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag |
由FeO、Fe2O3、Fe3O4组成的混合物,测得其中铁元素和氧元素的质量比为
,则这种混合物中FeO、Fe2O3、Fe3O4的物质的量之比可能为( )
| 21 |
| 8 |
| A、1:2:1 |
| B、2:1:1 |
| C、1:1:1 |
| D、1:2:3 |
与1.8g H2O含有相同氧原子数的H2SO4的质量为( )
| A、0.1 g |
| B、0.2 g |
| C、2.45 g |
| D、4.9 g |
在100mL HNO3和H2SO4的混合溶液中,两种酸的物质的量浓度之和为0.5mol/L.向该溶液中加入足量的铜粉,加热,充分反应后,所得溶液中Cu2+的物质的量浓度最大值为(反应前后溶液体积变化忽略不计)( )
| A、0.225mol/L |
| B、0.30mol/L |
| C、0.36mol/L |
| D、0.45mol/L |
下列反应中,不能用离子方程式 SO42-+Ba2+=BaSO4↓来表示的是( )
| A、稀硫酸与硝酸钡溶液反应 |
| B、硫酸钾溶液与氯化钡溶液反应 |
| C、稀硫酸与氢氧化钡溶液反应 |
| D、硫酸钠溶液与硝酸钡溶液反应 |
 目前工业上可用CO2来生产燃料甲醇,其反应方程式为:CO2(g)+
目前工业上可用CO2来生产燃料甲醇,其反应方程式为:CO2(g)+