物质在反应中可表现氧化性、还原性、酸性、碱性等,下面方程式中划线的物质,能在同一反应中同时表现上述两种或两种以上性质的有( )
①3FeO+10HNO3=3Fe(NO3)3+NO↑+5H2O
②C+2H2SO4(浓)=CO2↑+2SO2↑+2H2O
③8NH3+3Cl2=6NH4Cl+N2
④2Na2O2+2H2O=4NaOH+O2↑
①3FeO+10HNO3=3Fe(NO3)3+NO↑+5H2O
②C+2H2SO4(浓)=CO2↑+2SO2↑+2H2O
③8NH3+3Cl2=6NH4Cl+N2
④2Na2O2+2H2O=4NaOH+O2↑
| A、①②③ | B、①③④ |
| C、②③④ | D、全部 |
下面均是正丁烷与氧气反应的热化学方程式(25°,101kPa):
①C4H10(g)+
O2(g)=4CO2(g)+5H2O(l)△H=-2878kJ/mol
②C4H10(g)+
O2(g)=4CO2(g)+5H2O(g)△H=-2658kJ/mol
③C4H10(g)+
O2(g)=4CO(g)+5H2O(l)△H=-1746kJ/mol
④C4H10(g)+
O2(g)=4CO(g)+5H2O(g)△H=-1526kJ/mol
由此判断,正丁烷的燃烧热是( )
①C4H10(g)+
| 13 |
| 2 |
②C4H10(g)+
| 13 |
| 2 |
③C4H10(g)+
| 9 |
| 2 |
④C4H10(g)+
| 9 |
| 2 |
由此判断,正丁烷的燃烧热是( )
| A、-2878kJ/mol |
| B、-2658kJ/mol |
| C、-1746kJ/mol |
| D、-1526kJ/mol |
在一定温度下,将6mol C02和8mol H2充入2L恒容密闭容器中,发生反应:C02(g)+3H2(g)?CH30H(g)+H20(g) AH<O,一段时间后达到平衡.反应过程中测定的数据如下表.下列说法正确的是( )
| t/min | 1 | 4 | 8 | 11 |
| n(H2)/mol | 6 | 2.6 | 2 | 2 |
| A、反应前4min的平均速率v(C02)=0.45 mol/(L'min) |
| B、达到平衡时,H2的转化率为25% |
| C、其他条件不变,升高温度,反应达到新平衡时CH30H的体积分数增大 |
| D、该温度下,该反应的平衡常数为0.5 |
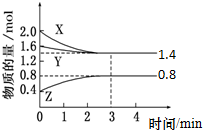 t℃时,在容积为2L密闭中充入X(g)、Y(g)与Z(g),反应过程中X、Y、Z的物质的量变化如下图所示.下列说法不正确的是( )
t℃时,在容积为2L密闭中充入X(g)、Y(g)与Z(g),反应过程中X、Y、Z的物质的量变化如下图所示.下列说法不正确的是( )| A、0~3 min,X的平均反应速率v(X)=0.1 mol?L-1?min-1 |
| B、发生反应的方程式可表示为:3 X(g)+Y(g)?2 Z(g) |
| C、3 min 时,Y的转化率为12.5%,此时,充入惰性气体Ne,转化率不变 |
| D、温度不变,增大Z的浓度,该反应的平衡常数增大 |

 某化学兴趣小组对碳的氧化物做了深入的研究并取得了一些成果.
某化学兴趣小组对碳的氧化物做了深入的研究并取得了一些成果.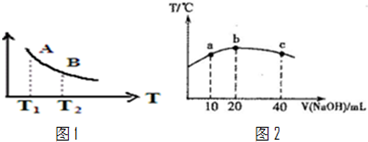
 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: