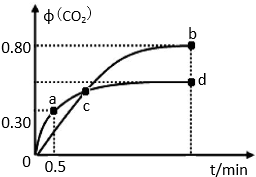
在温度T1和T2时,分别将0.50mol CH4和1.2mol NO2充入1L的密闭容器中发生反应:CH4(g)+2NO2(g)
N2(g)+CO2(g)+2H2O(g)△H=akJ/mol.测得有关数据如下表:下列说法正确的是( )
N2(g)+CO2(g)+2H2O(g)△H=akJ/mol.测得有关数据如下表:下列说法正确的是( )
| 温度 | 时间/min 物质的量 | 0 | 10 | 20 | 40 | 50 |
| T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | x | 0.15 |
| A、T1>T2,且a>0 |
| B、当温度为T2、反应进行到40 min时,x>0.15 |
| C、温度为T2时,若向平衡后的容器中再充入0.50 mol CH4和1.2mol NO2,重新达到平衡时,n(N2)=0.70mol |
| D、温度为T1时,若起始时向容器中充入0.50 mol CH4(g)、0.50 molNO2(g)、1.0 mol N2(g)、2.0 molCO2(g)、0.50 molH2O(g),反应开始时,ν(正)>ν(逆) |
下列四组离子中,不能在溶液中大量共存的是( )
| A、Na+、CO32-、Cl- |
| B、Ba2+、Na+、Cl- |
| C、H+、SO42-、OH- |
| D、Ag+、Al3+、NO3- |
在强酸溶液中,下列各组离子能够大量共存的是( )
| A、Mg2+、Ca2+、HCO3-、Cl- |
| B、Na+、AlO2-、Cl-、SO42- |
| C、Cu2+、Fe3+、Br-、MnO4- |
| D、K+、Fe3+、SO42-、NO3- |
将容积为50mL的量筒充满二氧化氮和氧气的混合气体,将量筒倒置在盛满水的水槽里,一段时间后,量筒里剩余气体体积为5mL.则原混合气体中NO2和O2体积比可能是( )
| A、9:1 | B、18:7 |
| C、41:9 | D、1:1 |
 N2O5是一种新型硝化剂,其性质和制备受到人们的关注.一定温度下,在2L固定容积的密闭容器中发生反应:2N2O5(g)?4NO2(g)+O2(g)△H>0.反应物和部分生成物的物质的量随反应时间变化的曲线如图所示.下列说法中,正确的是( )
N2O5是一种新型硝化剂,其性质和制备受到人们的关注.一定温度下,在2L固定容积的密闭容器中发生反应:2N2O5(g)?4NO2(g)+O2(g)△H>0.反应物和部分生成物的物质的量随反应时间变化的曲线如图所示.下列说法中,正确的是( )| A、0~20 s内平均反应速率v(N2O5)=0.1 mol?(L?s)-1 |
| B、曲线a表示NO2的物质的量随反应时间的变化 |
| C、10 s时,正、逆反应速率相等,达到平衡 |
| D、20 s时,正反应速率大于逆反应速率 |
下列气体是黄绿色的是( )
| A、Cl2 |
| B、N2 |
| C、SO2 |
| D、NO2 |
下列各组离子中,能在溶液中大量共存的是( )
| A、H+、Cl-、Na+、CO32- |
| B、Na+、Ag+、Cl-、NO3- |
| C、Cu2+、Mg2+、SO42-、Cl- |
| D、H+、Na+、Cl-、OH- |