砷是氮族元素,黄砷(As4)是其一种单质,其分子结构与白磷(P4)相似,以下关于黄砷与白磷的比较叙述正确的是( )
| A、分子中共价键键角均为60° |
| B、黄砷中共价键键能大于白磷 |
| C、分子中含有的共价键的数目都是4 |
| D、黄砷的熔点低于白磷 |
下列物质性质与应用对应关系正确的是( )
| A、二氧化锰具有还原性,可用于实验室制备氯气 |
| B、Na2O2能与水或二氧化碳反应生成氧气,可用作供氧剂 |
| C、碳酸氢钠能与碱反应,可用作食品的膨松剂 |
| D、Na2SO4浓溶液能使蛋白质发生盐析,可用于杀菌、消毒 |
短周期主族元素X、Y、Z、W的原子序数依次增大.X与W同主族,X、W的单质在标准状况下的状态不同.Y是空气中含量最高的元素,Z原子最外层电子数是其内层电子总数的3倍,Z2-与W+具有相同的电子层结构.下列说法正确的是( )
| A、原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X) |
| B、元素Y的简单气态氢化物的热稳定性比Z的强 |
| C、由X、Y、Z三种元素形成的化合物的水溶液可能呈碱性 |
| D、化合物X2Z2与W2Z2所含化学键类型完全相同 |
已知氧化还原反应:KClO3+6HCl═3Cl2↑+KCl+3H2O,下列说法正确的是( )
| A、Cl2是氧化产物,KCl是还原产物 |
| B、盐酸在该反应中只表现还原性 |
| C、每生成3 mol Cl2,有1 mol KClO3发生氧化反应 |
| D、每转移0.1 mol电子,能生成标准状况1344mLCl2 |
向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成.经查资料得知:Ag++2NH3?H2O?Ag(NH3)2++2H2O.下列分析不正确的是( )
| A、浊液中存在沉淀溶解平衡:AgCl (s)?Ag+(aq)+Cl-(aq) |
| B、实验可以证明NH3结合Ag+能力比Cl-强 |
| C、实验表明实验室可用氨水洗涤银镜反应后的试管 |
| D、由资料信息可推知:加浓硝酸后生成的沉淀为AgCl |

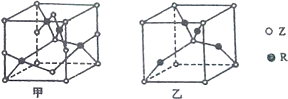 已知元素W、X、Y、Z、R为前四周期元素,且原子序数依次增大.元素W的负一价阴离子与某惰性气体结构相同,X是形成化合物种类最多的元素,Z原子L电子层上有2对成对电子,R+原子核外有3层电子且各层均处于全满状态.请回答下列问题:
已知元素W、X、Y、Z、R为前四周期元素,且原子序数依次增大.元素W的负一价阴离子与某惰性气体结构相同,X是形成化合物种类最多的元素,Z原子L电子层上有2对成对电子,R+原子核外有3层电子且各层均处于全满状态.请回答下列问题: