某同学在实验室中用KClO3代替MnO2制备Cl2,反应原理为KClO3+6HCl(浓)═KCl+3Cl2↑+3H2O.下列叙述不正确的是( )
| A、氧化剂为KClO3,其中Cl元素被还原 |
| B、若有3molH2O生成,则反应中有6mol电子转移 |
| C、浓HCl在反应中起酸性和还原性的作用 |
| D、氧化剂与还原剂的物质的量之比为1:5 |
在2Fe2++Cl2=2Fe3++2Cl-反应中,关于生成1molFe3+的说法正确的是( )
| A、Fe2+失去电子的物质的量为2 mol |
| B、Cl2得电子的物质的量为1 mol |
| C、参加反应的Cl2的物质的量为1mol |
| D、氧化剂与还原剂的物质的量之比为1:1 |
对于可逆反应H2(g)+I2(g)?2HI(g),在温度一定下由H2(g)和I2(g)开始反应,下列说法正确的是( )
| A、H2(g)的消耗速率与HI(g)的生成速率之比为2:1 |
| B、正、逆反应速率的比值是恒定的 |
| C、当HI的分子数与I2分子数之比为2:1时,说明反应达到了平衡状态 |
| D、达到平衡时,正、逆反应速率相等 |
下列变化中,属于被氧化的是( )
| A、CaO→Ca(OH)2 |
| B、Cu2+→Cu |
| C、Fe2+→Fe3+ |
| D、CO2→CO |
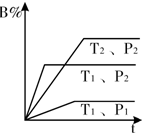 已知某可逆反应mA(g)+n B(g)?pC(g)△Η=Q在密闭容器中进行,如图中表示在不同反应时间t时,温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析下列判断正确的( )
已知某可逆反应mA(g)+n B(g)?pC(g)△Η=Q在密闭容器中进行,如图中表示在不同反应时间t时,温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析下列判断正确的( )| A、T1<T2 P1>P2 m+n>p Q<0 |
| B、T1>T2 P1<P2 m+n>p Q<0 |
| C、T1<T2 P1>P2 m+n<p Q>0 |
| D、T1>T2 P1<P2 m+n<p Q>0 |
在一密闭容器中,可逆反应aA(g)?bB(g)达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
| A、物质B的质量分数增大了 |
| B、物质A的转化率减小了 |
| C、平衡向逆反应方向移动了 |
| D、a>b |
反应3Fe(s)+4H2O (g)
Fe3O4(s)+4H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
| ||
| A、增加铁的量 |
| B、将容器体积缩小一半 |
| C、升高温度 |
| D、压强不变,充入N2使容器体积增大 |
下列物质中,属于电解质的是( )
| A、NaOH | B、蔗糖 |
| C、稀盐酸 | D、NaCl溶液 |
下列物质属于电解质且又能导电的是( )
| A、硝酸钾溶液 |
| B、液态的氯化氢 |
| C、熔融的氯化钠 |
| D、金属铜 |