下列事实得出的结论正确的是( )
| A、可用加热法除去氯化钠固体中的氯化铵杂质 |
| B、只用铜片不能鉴别浓硝酸和稀硝酸 |
| C、常温下,Al和浓硫酸钝化说明Al和浓硫酸在常温下不反应 |
| D、SO2通入氯化钡溶液无现象,若再通入NH3或NO2气体则都会产生BaSO4的白色沉淀 |
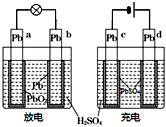 已知蓄电池在充电时作电解池,放电时作原电池.如图是铅蓄电池的工作示意图,其反应原理为:PbO2+Pb+2H2SO4
已知蓄电池在充电时作电解池,放电时作原电池.如图是铅蓄电池的工作示意图,其反应原理为:PbO2+Pb+2H2SO4| 放电 |
| 充电 |
| A、b电极放电后转化为c电极 |
| B、电极a和d都发生还原反应 |
| C、b的电极反应式:Pb+SO42--2e→PbSO4 |
| D、放电后硫酸溶液的pH增大 |
下列关于核外电子的描述中,正确的是( )
| A、电子云图中一个小黑点表示一个电子 |
| B、电子式中元素符号周围的小黑点数表示核外电子总数 |
| C、s电子在s电子云的球形空间内做规则运动 |
| D、核外电子的能量大小主要是由电子层和电子亚层决定 |
a、b、c三种短周期金属元素,原子序数依次增大,单质的物质的量分别为n(a)、n(b)、n(c),它们与足量盐酸反应产生的氢气体积(标准状况下)为V(H2)a、V(H2)b、V(H2)c.当n(a)=n(b)=n(c),则2V(H2)a=V(H2)b+V(H2)c,下列说法中正确的是( )
| A、a、b、c可能是同周期元素 |
| B、a可能是镁元素 |
| C、b、c两者的最高价氧化物对应的水化物能反应 |
| D、工业上冶炼b、c通常是用电解法制得 |
下列物质加热熔化时破坏极性共价键的是( )
| A、干冰 | B、晶体硅 |
| C、氢氧化钠 | D、二氧化硅 |
用石墨作电极电解0.1mol?L-1的CuSO4溶液,当有0.4mol电子通过电路时,发现阴极增重6.4g,则要使电解后的溶液恢复到原始状态,则应向电解后的溶液中加入( )
| A、0.1molCu(OH)2 |
| B、0.1molCuO |
| C、0.2molCuO |
| D、0.1molCuO和0.2molH2O |
人工肾脏可用间接电化学方法除去代谢产物中的尿素,原理如图.下列有关说法正确的是( )

| A、a为电源的负极 |
| B、电解结束后,阴极室溶液的pH与电解前相比将升高 |
| C、阳极室中发生的电极反应为2H++2e-=H2↑ |
| D、若两极共收集到气体13.44L(标准状况),则除去的尿素为7.2g(忽略气体的溶解) |
室温下,下列溶液说法正确的是( )
| A、pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| B、0.1mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-) |
| C、pH=5的H2S溶液中,c(H+)=c(HS-)=1×10-5 mol?L-1 |
| D、CH3COONa和CaCl2混合溶液:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-) |
 光气(COCl2)、联氨(N2H4)和H2O2具有重要的工业价值.
光气(COCl2)、联氨(N2H4)和H2O2具有重要的工业价值.