下列叙述正确的是( )
| A、SiO2可用于制备光导纤维 |
| B、MgO和Al2O3均只能与酸反应,不能与碱反应 |
| C、液氯就是氯气的水溶液,它能使干燥的有色布条褪色 |
| D、Mg和Fe在一定条件下与水反应都生成H2和对应的碱 |
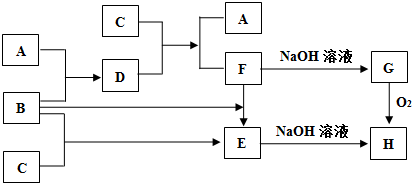
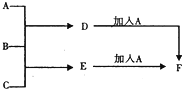 A、B、C为3种单质(其中A为固体,B、C为气体),将D的饱和溶液滴人沸水中继续煮沸,溶液呈红褐色,B、C反应的产物易溶于水得到无色溶液E.它们之间的转化关系如图,下列推断正确的是( )
A、B、C为3种单质(其中A为固体,B、C为气体),将D的饱和溶液滴人沸水中继续煮沸,溶液呈红褐色,B、C反应的产物易溶于水得到无色溶液E.它们之间的转化关系如图,下列推断正确的是( )| A、物质B是H2 |
| B、物质C是Cl2 |
| C、物质D是FeCl2 |
| D、物质F是FeCl2 |
 一定温度下,在2L固定容积的密闭容器中发生反应:2N2O5(g)?4NO2(g)+O2(g)△H>0.反应物和部分生成物的物质的量随反应时间变化的曲线如图所示.下列说法中,正确的是( )
一定温度下,在2L固定容积的密闭容器中发生反应:2N2O5(g)?4NO2(g)+O2(g)△H>0.反应物和部分生成物的物质的量随反应时间变化的曲线如图所示.下列说法中,正确的是( )| A、20 s时,正反应速率大于逆反应速率 |
| B、10 s时,正、逆反应速率相等,达到平衡 |
| C、a曲线是NO2的物质的量随反应时间的变化曲线 |
| D、0~20 s内平均反应速率v(N2O5)=0.1 mol?(L?s)-1 |
现有乙烯、氯气和必要的试剂,若要在适当条件下制取1,1,2,2-四氯乙烷,则这一过程中所要经历的反应及耗用氯气的物质的量分别是(设乙烯的物质的量为1mol)( )
| A、取代,4 mol Cl2 |
| B、加成,2mol Cl2 |
| C、加成,取代,3 mol Cl2 |
| D、加成,消去,取代,3 mol Cl2 |
 LiAlH4由Li+、A1H4一构成,是有机合成中常用的还原剂.
LiAlH4由Li+、A1H4一构成,是有机合成中常用的还原剂.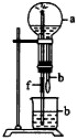 如图,烧瓶中充满干燥气体a,胶头滴管及烧杯中均为液体b,挤压胶头滴管,然后打开弹簧夹f,烧瓶中出现喷泉,最后烧瓶充满b.下列不符合上述条件的是( )
如图,烧瓶中充满干燥气体a,胶头滴管及烧杯中均为液体b,挤压胶头滴管,然后打开弹簧夹f,烧瓶中出现喷泉,最后烧瓶充满b.下列不符合上述条件的是( ) 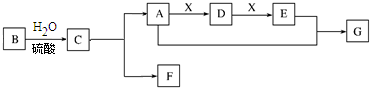
 按要求回答下列问题:
按要求回答下列问题: