下列物质的名称、俗名与化学式完全对应的是( )
| A、氯化钠 食盐 NaCl2 |
| B、碳酸氢钠 纯碱 NaHCO3 |
| C、氢氧化钙 熟石灰 CaO |
| D、氢氧化钠 烧碱 NaOH |
下列有关化学用语表示正确的是( )
A、H2S的电子式: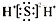 |
B、基态氧原子的电子排布图: |
| C、二氧化硅的分子式:SiO2 |
| D、24Cr的电子排布式:[Ar]3d54s1 |
铊是超导材料的组成元素之一,铊在元素周期表中位于第六周期,与铝是同主族元素,元素符号是Tl.以下对铊的单质及其化合物的性质推断不正确的是( )
| A、铊是易导电的银白色金属 |
| B、能生成+3价离子 |
| C、氢氧化铊是两性氢氧化物 |
| D、Tl3+的氧化能力比Al3+强 |
下列有关主族元素形成的离子的叙述正确的是( )
| A、单核阳离子的电子层结构(除氢外)一定与上一周期稀有气体原子相同 |
| B、单核阳离子的电子层数一定比其他原子的电子层数少 |
| C、单核阴离子的半径一定比其原子半径大 |
| D、单核阴离子最外层一定是八电子结构 |
下列说法中错误的是( )
| A、根据对角线规则,铍和铝的性质具有相似性 |
| B、[Cu(H2O)4]2+中Cu提供空轨道,H2O中O提供孤对电子形成配位键 |
| C、元素电负性越大的原子,吸引电子的能力越强 |
| D、手性分子互为镜像,它们的性质没有区别 |
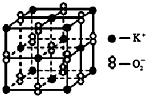 高温下,超氧化钾晶体(KO2)呈立方体结构(与NaCl晶体结构相似).如图为超氧化钾晶体的一个晶胞.则有关下列说法不正确的是( )
高温下,超氧化钾晶体(KO2)呈立方体结构(与NaCl晶体结构相似).如图为超氧化钾晶体的一个晶胞.则有关下列说法不正确的是( )| A、KO2中既存在离子键也存在共价键 |
| B、一个KO2晶胞中摊得的K+和O2-粒子数均为4个 |
| C、晶体中与每个K+距离最近的O2-有8个 |
| D、与K+距离相等且最近的K+有12个 |
下列化合物中,既含有离子键又含有共价键的是( )
| A、HBr |
| B、CO2 |
| C、CaCl2 |
| D、NaOH |
短周期元素A、B、C、D、E,原子序数依次增大.已知元素A的气态氢化物和A的最高价氧化物对应的水化物反应生成盐;B、E为同主族元素,B元素原子最外层电子数是次外层的3倍;D是地壳中含量最多的金属元素;C是短周期中与水反应最激烈的金属元素.下列叙述不正确的是( )
| A、元素A的氧化物常温下一般均为无色无味气体 |
| B、元素C、D、E的最高价氧化物对应的水化物两两之间能发生反应 |
| C、原子半径:C>D>B |
| D、元素B的气态氢化物的沸点比元素E气态氢化物的沸点高 |
钠元素与硅元素最本质的区别是( )
| A、质子数不同 |
| B、相对原子质量不同 |
| C、中子数不同 |
| D、最外层电子数不同 |
下列选项中发生了化学变化的是( )
| A、木料制家具 | B、大米酿酒 |
| C、石蜡熔化 | D、水制冰块 |