下列说法不正确的是( )
| A、某化验单标有:总胆红素12.3μmol/L,其表示的物理量是物质的量浓度 |
| B、20gNaOH溶于1L水,可配得0.5mol/LNaOH溶液 |
| C、同温同压下,11gCO2气体与32gSO2气体的体积比为1:2 |
| D、100mL0.1mol/L盐酸中含有的氯离子数约为6.02×1021 |
下列有关化学用语的表示正确的是( )
A、甲烷分子的球棍模型: | ||
| B、乙炔的实验式:CH | ||
C、中子数为16的硫原子:
| ||
D、间二甲苯的结构简式: |
下列说法正确的是( )
| A、RO3-与R-可发生反应:RO3-+5R-+6H+══3R2+3H2O,元素R位于周期表中第ⅤⅡA族 |
| B、短周期主族元素的最高价等于最外层电子数 |
| C、原子序数越大原子半径越大,离子半径越小 |
| D、第三周期元素随原子序数增大,含氧酸的酸性增强 |
化学反应前后肯定不变的是( )
| A、物质的种类 |
| B、原子的种类和数目 |
| C、分子的种类 |
| D、分子的数目 |
常温下,向100mL3mol?L-1的氢氧化钾溶液中通入标准状况下4.48L的硫化氢气体,充分反应后得到稳定的溶液,已知KHS溶液呈碱性,选项中正确的是( )
| A、该溶液中K2S的浓度为2mol?L-1 |
| B、C(K+)+C(H+)═C(HS-)+C(S2-)+C(OH-) |
| C、该溶液中水的电离程度大于常温下纯水的电离程度 |
| D、C(K+)>c(S2-)>C(HS-)>c(OH-)>C(H+) |
下列说法正确的是( )
| A、同温同压下,相同体积的物质,其物质的量一定相等 |
| B、标准状况下气体摩尔体积约为22.4L |
| C、0.5 L 1 mol/L FeCl3溶液与0.2 L 1 mol/L KCl溶液中的Cl-的数目之比为15:2 |
| D、150 mL 1 mol/L NaCl溶液与50 mL 1 mol/L AlCl3溶液中Cl-物质的量浓度相等 |
下列有关晶体的叙述,错误的是( )
| A、金刚石的网状结构中,由共价键形成的最小碳环上有6个碳原子 |
| B、在NaCl晶体中,每个Na+(或Cl-)周围都紧邻有6个Cl-(或Na+) |
| C、干冰晶体中,粒子之间通过共价键结合 |
| D、离子晶体在熔化时,离子键被破坏,而分子晶体熔化时,化学键不被破坏 |
下列排列顺序不正确的是( )
| A、原子半径:Si>Na>O |
| B、热稳定性:HF>HCl>H2S |
| C、碱性:CsOH>KOH>NaOH |
| D、失电子能力:K>Na>Mg |
如图所示,A、B、C、D、E是元素周期表中的5种主族元素,下列说法不正确的是( )
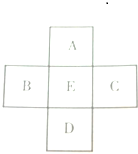

| A、A、E原子序数之差可能为2 |
| B、D、E原子序数之差可能为18或32 |
| C、B、C原子序数之差一定是2 |
| D、B、D原子序数之差不可能是7 |