氯气用途十分广泛,可用于生产半导体材料硅,其生产的流程如下,下列说法不正确的是( )石英砂
粗硅
四氯化硅
纯硅.
| ①焦炭 |
| 高温 |
| ②氯气 |
| 加热 |
| ③氢气 |
| 高温 |
| A、①③是置换反应,②是化合反应 |
| B、高温下,焦炭与氢气的还原性均强于硅 |
| C、任一反应中,每消耗或生成28 g硅,均转移4 mol电子 |
| D、如果焦炭不足,反应①会释放CO2气体 |
工业上可用“四室电渗析法”制备一元中强酸H3PO2,工作原理如图所示,图中X、Y代表阳膜或阴膜,阳膜和阴膜分别只允许阳离子、阴离子通过,电极M和N材质均为石墨.下列说法错误的是( )


| A、NaH2PO2溶液一定呈碱性 |
| B、图中X为阳膜,Y为阴膜 |
| C、电极M上的反应为:4OH --4e-=O2↑+2H2O |
| D、电解过程中,H+会从阳极室穿过X膜扩散至产品室,Na+会从阴极室扩散至原料室 |
酸HX的下列性质中,可以证明它是弱电解质的是( )
| A、1 mol/L HX溶液的pH值约为2 |
| B、HX能与水以任意比例互溶 |
| C、10 mL 1mol/L HX恰好与10 mL l mol/L NaOH溶液完全反应 |
| D、HX溶液的导电性比强酸溶液的弱 |
下列过程通电后才能进行的是( )
①电离 ②电解 ③电镀 ④电化学腐蚀.
①电离 ②电解 ③电镀 ④电化学腐蚀.
| A、②③ | B、①②④ |
| C、②③④ | D、全部 |
在常温下,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A、弱酸性NaHSO3溶液:c(HSO3-)>c(Na+)>c(H+)>c(OH-) |
| B、0.1mol/LNH4HS溶液:c(NH4+)=c(HS-)+c(H2S)+c(S2-) |
| C、0.2 mol/LNH3?H2O溶液与0.1mol/L盐酸等体积混合:c(NH4+)>c(C1-)>c(OH-)>c(H+) |
| D、0.2mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合:(H+)=c(OH-)+c(HCO3-)+2c(H2CO3) |
化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
| A、铝盐(明矾溶液)和铁盐(硫酸铁溶液)都有净水作用,两者的作用原理是相同的 |
| B、放在冰箱中的食品保质期较长,这与温度对反应速率的影响有关 |
| C、0.1mol/L的CH3COONa溶液的pH约为9,说明CH3COOH是弱酸 |
| D、室温下向10mLpH=3的醋酸溶液中加入水稀释后,溶液中导电粒子的数目减少 |
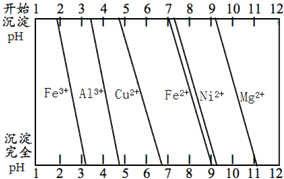 关于金属的冶炼和应用,有以下一些问题,请按要求回答问题.
关于金属的冶炼和应用,有以下一些问题,请按要求回答问题.