反应2A(g)?2B(g)+C(g)△H>0,达平衡时,要使v正降低、c(A)增大,应采取的措施是( )
| A、加压 | B、减压 |
| C、减小C的浓度 | D、降温 |
已知反应:①C+CO2?2CO△H>0 ②N2+3H2?2NH3△H<0.达平衡后升温,正反应速率的变化是( )
| A、①加快,②减慢 |
| B、均加快 |
| C、均减慢 |
| D、①减慢,②加快 |
某恒温恒容的容器中,建立如下平衡:2NO2(g)?N2O4(g),在相同条件下,若分别向容器中通入一定量的NO2气体或N2O4气体,重新达到平衡后,容器内N2O4的体积分数比原平衡时( )
| A、都增大 |
| B、都减小 |
| C、前者增大后者减小 |
| D、前者减小后者增大 |
下列事实不能用勒夏特列原理解释的是( )
| A、热的纯碱去污效果更好 |
| B、在H2、I2和HI组成的平衡体系加压后,混合气体颜色变深 |
| C、实验室可用排饱和食盐水的方法收集氯气 |
| D、高压下有利于提高合成氨的产率 |
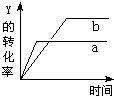 反应 X(气)+Y(气)?2Z(气)+Q(Q>0),在一定条件下,反应物Y的转化率与反应时间(t)的关系如图所示.若使曲线a变为曲线b可采取的措施是( )
反应 X(气)+Y(气)?2Z(气)+Q(Q>0),在一定条件下,反应物Y的转化率与反应时间(t)的关系如图所示.若使曲线a变为曲线b可采取的措施是( )| A、加入催化剂 | B、降低温度 |
| C、增大压强 | D、增大Y的浓度 |
对于可逆反应:mA(g)+nB(g)?xC(g)+yD(s)△H=?,在不同温度及压强(P1,P2)条件下,反应物A的转化率如图所示,下列判断正确的是( )


| A、△H>0,m+n>x+y |
| B、△H<0,m+n>x+y |
| C、△H<0,m+n>x |
| D、△H>0,m+n<x |
25℃时,下列溶液中,离子浓度关系正确的是( )
| A、pH=a的氨水稀释10倍后,其pH=b,则a=b+1 |
| B、浓度相同的①NH4Cl ②CH3COONH4③NH4HSO4,三种溶液中的c(NH4+):①>③>② |
| C、将相同浓度的氨水与盐酸等体积混合,所得溶液中的离子浓度关系:c (NH4+)>c (Cl-)>c (H+)>c (OH-) |
| D、将a mol?L-1CH3COOH与b mol?L-1NaOH溶液等体积混合,测得溶液pH为7,则a与b的关系:a>b |
有①NaOH溶液②Na2CO3溶液③CH3COONa溶液各10mL,物质的量浓度均为0.1mol?L-1,下列说法正确的是( )
| A、三种溶液pH的大小顺序是①>③>② |
| B、若分别加入10mL 0.1mol?L-1盐酸后,pH最大的是② |
| C、若将三种溶液稀释相同倍数,pH变化最大的是③ |
| D、三种溶液中由水电离出的OH-浓度的大小顺序是①>②>③ |
下列叙述正确的是( )
| A、常温时,某溶液中由水电离出来的c(H+)和c(OH-)的乘积为1×10-24,该溶液中一定可以大量存在K+、Na+、AlO2-、SO42- | ||
B、常温时,0.1mol/L HA溶液的pH>1,0.1mol/L BOH溶液中
| ||
| C、将等浓度的K2S和KHSO4两种溶液等体积,则混合溶液中离子浓度的大小关系为:c(K+)>c(SO42-)>c(HS-)>c(OH-)>c(H+)>c(S2-) | ||
| D、常温下,Cd(OH)2和Co(OH)2的混合悬浊液中,c(Cd2+)是c(Co2+)的3.5倍(已知:Ksp(Cd(OH)2)=7.2×10-15,Ksp(Co(OH)2)=1.8×10-15) |