有机物A(化学式为C4H8O3)在一定条件下的性质有:在浓硫酸存在下,可脱水生成能使溴水褪色的只有一种结构形式的有机物B;在浓硫酸存在下,能分别与乙醇或乙酸反应生成有机物C或D;在浓硫酸存在下,还能生成分子式为C8H12O4的六元环状有机物E.则下列有关叙述一定正确的( )
| A、有机物A的名称为α-羟基丁酸 |
| B、有机物B的结构简式可能为CH3CH=CHCOOH |
| C、有机物C和D属同分异构体 |
| D、环状有机物E的结构只有一种 |
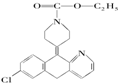 开瑞坦是治疗过敏性鼻炎的良药,其有效成分的结构简式如图所示,下列关于该有机物的说法正确的是( )
开瑞坦是治疗过敏性鼻炎的良药,其有效成分的结构简式如图所示,下列关于该有机物的说法正确的是( )| A、该有机物的分子式是C21H22N2O2Cl |
| B、分子中含有四个六元环,其中有一个是苯环 |
| C、1mol分子发生水解反应后能得到2mol新分子 |
| D、1mol分子发生加成反应需要8molH2 |
根据以下几个反应:判断还原性由强到弱的顺序是( )
①Cl2+2KI═2KCl+I2
②2FeCl2+Cl2═2FeCl3
③2FeCl3+2KI═2FeCl2+2KCl+I2
④I2+SO2+2H2O═H2SO4+2HI.
①Cl2+2KI═2KCl+I2
②2FeCl2+Cl2═2FeCl3
③2FeCl3+2KI═2FeCl2+2KCl+I2
④I2+SO2+2H2O═H2SO4+2HI.
| A、I->Fe2+>SO2>Cl- |
| B、SO2>Fe2+>I->Cl- |
| C、SO2>I->Fe2+>Cl- |
| D、Fe2+>I->Cl->SO2 |
分类是化学研究中常用的方法.下列分类方法正确的是( )
| A、根据溶液酸碱性,将化合物分为酸、碱、盐 |
| B、根据分散质微粒直径大小,将分散系分为胶体、浊液和溶液 |
| C、根据水溶液是否导电,将化合物分为电解质和非电解质 |
| D、根据化合物是否来自于有机体,将化合物分为有机物和无机物 |
设NA代表阿伏加德罗常数的值.下列说法不正确的是( )
| A、含NA个铜原子的CuO和Cu2S的混合物质量为80.0 g |
| B、标准状况下,22.4 L氧气作氧化剂时转移电子数为4NA |
| C、500 mL、2 mol?L-1碳酸钠溶液中带电粒子数一定大于3NA |
| D、50 mL 18 mol?L-1浓硫酸与足量锌粒反应,产生的气体分子数小于0.9NA |
下列物质的分类正确的是( )
| A、常见的氧化物:水、氧化铜、熟石灰 |
| B、分散系-空气、水玻璃、盐酸 |
| C、非电解质-液氯、乙醇、NH3 |
| D、强氧化剂-盐酸、硫酸、硝酸 |
用NA表示阿伏德罗常数,下列叙述正确的是( )
| A、标准状况下将 22.4LHCl溶于水所得的盐酸中含有NA个HCl分子 |
| B、常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA |
| C、通常状况下,用含1 molFeCl3的饱和溶液可以制得含NA个Fe(OH)3胶粒的Fe(OH)3胶体 |
| D、物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为 NA |
设NA代表阿伏加德罗常数,下列说法正确的是( )
| A、常温常压下,1 mol氢气中含有NA个氢原子 |
| B、5.6g Fe与足量的盐酸反应转移电子数为0.2NA |
| C、标准状况下,体积2.24L水中含有水分子数为0.1mol |
| D、46g NO2和N2O4的混合物含有分子数为NA |
pH=2的盐酸和pH=12的NaOH溶液等体积混合后,溶液的pH值是( )
| A、5.0 | B、7.0 |
| C、1.0 | D、14 |