向恒温恒容密闭容器中加入1molHI,发生下列反应2HI(g)═H2(g)+I2(g),△H>0.达到平衡后,往容器中再加入1molHI,有关说法正确的是( )
| A、平衡不移动,HI平衡转化率不变 |
| B、平衡向右移动,HI平衡转化率不变 |
| C、平衡向左移动,HI平衡转化率减小 |
| D、平衡向右移动,HI平衡转化率增大 |
现将足量的AgCl固体分别放入下列物质中,所得溶液中c(Ag+)最小是( )
| A、10 mL 0.2mol?L-1MgCl2溶液 |
| B、20 mL 0.5 mol?L-1 AgNO3溶液 |
| C、40 mL 0.3mol?L-1HCl溶液 |
| D、15 mL 0.1mol?L-1 AlCl3溶液 |
在10L密闭容器中,A、B、C三种气态物质构成了可逆反应的体系;当在某一温度时,A、B、C物质的量与时间的关系如图一,C的百分含量与温度的关系如图二.

下列分析不正确的是( )

下列分析不正确的是( )
| A、0~4分钟时,A的速率为0.01mol/(L?min) | ||
| B、由T1向T2变化时,V正>V | ||
C、该反应的平衡常数表达式K=
| ||
| D、此反应的正反应为吸热反应. |
下列实验操作过程中需要使用圆底烧瓶的是( )
| A、过滤 | B、蒸馏 | C、溶解 | D、分液 |
漂白粉在空气中容易变质的原因是( )
| A、CaCl2易吸收空气中的水分 |
| B、Ca(ClO)2易与盐酸反应 |
| C、Ca(ClO)2见光易分解 |
| D、Ca(ClO)2易与空气中的CO2和水作用 |
欲除去下列物质中混入的少量杂质(括号内物质为杂质),错误的是( )
| A、乙酸乙酯(乙酸):加饱和Na2CO3溶液,充分振荡静置后,分液 |
| B、乙醇(水):加入新制生石灰,蒸馏 |
| C、溴苯(溴):加入NaOH溶液,充分振荡静置后,分液 |
| D、乙酸(乙醇):加入金属钠,蒸馏 |
下列实验操作中错误的是( )
| A、分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C、碘易溶于酒精,因此可用酒精萃取碘水中的碘 |
| D、称量NaCl时,NaCl放在称量纸上,置于托盘天平的左盘,砝码放在托盘天平的右盘 |
下列说法中,不正确的是( )
| A、分液操作时,分液漏斗下端管口尖端处紧靠烧杯内壁 |
| B、利用丁达尔效应可鉴别溶液和胶体 |
| C、二氧化硅能用于制造光导纤维 |
| D、用pH试纸测定某溶液的pH时,需预先用蒸馏水湿润pH试纸 |
在298K、100kPa时,已知:
Cl2(g)+H2(g)═2HCl(g)△H1、2H2O(g)═2H2(g)+O2(g)△H2、2Cl2(g)+2H2O(g)═4HCl(g)+O2(g)△H3 则△H3与△H2和△H1之间的关系正确的是( )
Cl2(g)+H2(g)═2HCl(g)△H1、2H2O(g)═2H2(g)+O2(g)△H2、2Cl2(g)+2H2O(g)═4HCl(g)+O2(g)△H3 则△H3与△H2和△H1之间的关系正确的是( )
| A、△H3=2△H1-△H2 |
| B、△H3=△H1+△H2 |
| C、△H3=2△H1+△H2 |
| D、△H3=△H2-△H1 |
某一容器中发生如下反应:2NO(g)+O2(g)═2NO2(g);△H=Q kJ?mol-1在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的关系如图所示.下列判断正确的是( )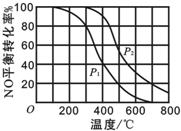

| A、p2>p1且Q<0 |
| B、p2>p1且Q>0 |
| C、p2<p1且Q<0 |
| D、p2<p1且Q>0 |