短周期元素X、Y、Z、W、U原子序数依次递增.X与W位于同一主族,Z元素的单质既能与盐酸反应也能与NaOH溶液反应,W原子的最外层电子数是次外层电子数的一半,Z、W、U原子的最外层电子数之和为13.Y元素的单质在X的某种氧化物中可燃.下列说法正确的是( )
| A、X、W、U的最高价氧化物对应的水化物酸性由强到弱的顺序为:U>W>X |
| B、Y、Z元素的单质作电极,在NaOH溶液中构成原电池,Z电极上产生大量气泡 |
| C、室温下,0.05 mol/L U的气态氢化物的水溶液的pH>1 |
| D、Y、Z、U元素的简单离子半径由大到小的顺序:Y>Z>U |
含NO3-的工业废水会造成水体富营养化,可利用如下反应将其转化为无毒、无污染的N2:A1+口+口→口十口+口,反应中涉及到的另外3种微粒是H2O、A1(OH)3、OH-.下列说法正确的是( )
| A、反应中的Al被还原,NO3-是还原剂 |
| B、三种反应物分别是Al、NO3-和OH- |
| C、若有1 mol Al参加反应,则有0.6 mol NO3-被还原 |
| D、随着反应的进行,溶液的碱性逐渐减弱 |
下列关于电子层或原子轨道类型的说法中,不正确的是( )
| A、原子核外电子的每一个电子层最多可容纳的电子数为2n2 |
| B、任一电子层原子轨道总是从s轨道开始,而且原子轨道类型数目等于该电子层序数 |
| C、同是s轨道,在不同的能层中,所能容纳的最多电子数不同 |
| D、一个原子轨道里最多只能容纳2个电子 |
在反应2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O中,有0.8mol HCl参与反应,则电子转移的个数为( )
| A、3.01×1023 |
| B、4.816×1023 |
| C、6.02×1023 |
| D、1.204×1024 |
根据下列反应判断有关物质的还原性由强到弱的顺序正确的是( )
①H2SO3+I2+H2O═2HI+H2SO4
②2FeCl3+2HI═2FeCl2+2HCl+I2
③3FeCl2+4HNO3═2FeCl3+NO↑+2H2O+Fe(NO3)3.
①H2SO3+I2+H2O═2HI+H2SO4
②2FeCl3+2HI═2FeCl2+2HCl+I2
③3FeCl2+4HNO3═2FeCl3+NO↑+2H2O+Fe(NO3)3.
| A、H2SO3>I->Fe2+>NO |
| B、I->H2SO3>Fe2+>NO |
| C、Fe2+>I->H2SO3>NO |
| D、NO>Fe2+>H2SO3>I- |
下列各图中,表示正反应是吸热反应的图是( )
A、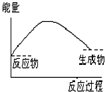 |
B、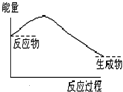 |
C、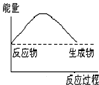 |
D、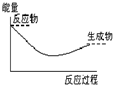 |
据美国《科学》杂志报道,外太空的某一星球的大气层中,含有大量的CH2=CHOH,此物质常温时为液体,它很容易转化成CH3CHO,化学方程式为CH2=CHOH?CH3CHO;已知△H<0.据此你认为下列说法中错误的是( )
| A、该星球表面温度很高 |
| B、该星球表面温度很低 |
| C、该反应为放热反应 |
| D、高温下稳定性CH2=CHOH>CH3CHO |
常见镍氢电池的某极是储氢合金LaNi5H6 (LaNi5H6中各元素化合价均为零),电池反应通常表示为LaNi5H6+6NiO(OH)2
LaNi5+6Ni(OH)3下列说法不正确的是( )
| 放电 |
| 充电 |
| A、放电时储氢合金作负极 |
| B、充电是将电能转化为化学能的过程 |
| C、充电时储氢合金作阴极 |
| D、1mol LaNi5H6参加放电,能提供12mol电子 |
 固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的.它以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )
固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的.它以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是( )| A、有O2放电的a极为电池的负极 |
| B、O2-移向电池的正极 |
| C、b极对应的电极反应为2H2-4e-+2O2-═2H2O |
| D、a极对应的电极反应为O2+2H2O+4e-═4OH- |