测得室温下0.1mol?L-1的某酸HA溶液的PH=3,下列叙述错误的是( )
| A、HA是弱酸 |
| B、若升高温度,溶液的PH增大 |
| C、此酸的电离平衡常数约为10-5 |
| D、由HA电离出的c(H+)约为水电离出的c(H+)的108倍 |
工业上正在研究利用C02来生产甲醇燃料,该方法的化学方程式为C02(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,一定温度下,在三个容积均为3.OL的恒容密闭容器中发生该反应:下列有关说法不正确的是( )
| 容器 | 起始物质的量/mol | 平衡物质的量/mol | |||
| 编 号 | 温度/℃ | C02 (g) | H2(g) | CH3OH(g) | H2 O(g) |
| I | T1 | 3 | 4 | O.5 | O.5 |
| Ⅱ | T1 | 1.5 | 2 | ||
| Ⅲ | T2 | 3 | 4 | O.8 | O.8 |
| A、若经过2min容器I中反应达平衡,则2min内平均速率(H2)=O.25 mol/(L?min) |
| B、达到平衡时,容器I中C02转化率的比容器Ⅱ的大 |
| C、达到平衡时,容器Ⅲ中反应放出的热量比容器Ⅱ的2倍少 |
| D、若容器I、Ⅱ、Ⅲ中对应条件下的平衡常数分别为K1、K2、K3,则K1=K2<K3 |
下列有关说法正确的是( )
| A、在300℃、70MPa下由二氧化碳和氢气合成乙醇已成为现实.2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g),则可推测该反应是吸热反应 | ||
| B、锅炉中沉积的CaSO4可用饱和Na2CO3溶液浸泡后再用酸溶解去除 | ||
C、室温下,将浓度为0.1mol.L?1HF溶液加水稀释,其电离平衡常数和
| ||
| D、电解精练铜时,阳极泥中常含有金属金、银、锌等 |
下列两种气体的分子数一定相等的是( )
| A、质量相等而密度不等的N2和CO |
| B、等体积、等密度的CO和NO |
| C、等温、等体积的N2 和O2 |
| D、等压、等体积的N2和CO2 |
气体A与B的摩尔质量之比为4:1,则它们在同温同压同体积时A与B的分子个数之比为( )
| A、4:1 | B、1:4 |
| C、1:1 | D、1:2 |
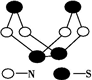 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法中正确的是( )
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法中正确的是( )| A、该物质的摩尔质量为46 g?mol-1 |
| B、1 mol该物质含有9个共价键 |
| C、相同质量的该物质和S2N2所含原子个数之比为1:1 |
| D、该物质与S2N2互为同分异构体 |
下列物质中,属于共价化合物的是( )
| A、NH4Cl |
| B、HN03 |
| C、NaCl |
| D、I2 |
X、Y、Z、W为四种短周期主族元素,它们在周期表中的位置如图所示.Z元素原子核外K层与M层电子数相等.下列说法中正确的是( )
| X | Y | ||
| Z | W |
| A、Y元素最高价氧化物对应的水化物化学式为H3YO4 |
| B、原子半径由小到大的顺序为X<Z<Y<W |
| C、与同浓度的盐酸反应,Z比W 更剧烈 |
| D、X、Z两种元素氧化物中所含化学键的类型相同 |
金属键的形成是通过( )
| A、金属原子与自由电子之间的相互作用 |
| B、金属离子与自由电子之间强烈的相互作用 |
| C、自由电子之间的相互作用 |
| D、金属离子之间的相互作用 |