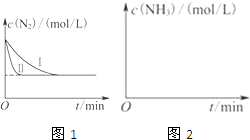
下列图示关系中不正确的是( )
A、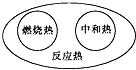 |
B、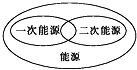 |
C、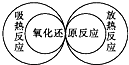 |
D、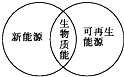 |
氧化钙是碱性氧化物,下列关于氧化钙性质叙述不正确的是( )
| A、氧化钙可以与水反应生成碱 |
| B、氧化钙可以与盐酸反应 |
| C、氧化钙可以和Na2O反应 |
| D、氧化钙可以与CO2反应 |
已知2-丁烯有顺、反两种异构体,在某条件下两种气体处于平衡:下列有关说法正确的是( )
①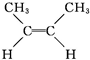 (g)?
(g)?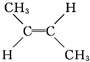 (g)△H=-4.2kJ?mol-1
(g)△H=-4.2kJ?mol-1
顺-2-丁烯 反-2-丁烯
②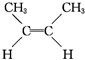 (g)+H2(g)→CH3CH2CH2CH3(g)△H=-118.9kJ?mol-1.
(g)+H2(g)→CH3CH2CH2CH3(g)△H=-118.9kJ?mol-1.
①
 (g)?
(g)? (g)△H=-4.2kJ?mol-1
(g)△H=-4.2kJ?mol-1顺-2-丁烯 反-2-丁烯
②
 (g)+H2(g)→CH3CH2CH2CH3(g)△H=-118.9kJ?mol-1.
(g)+H2(g)→CH3CH2CH2CH3(g)△H=-118.9kJ?mol-1.| A、顺-2-丁烯比反-2-丁烯稳定 |
| B、1 mol反-2-丁烯完全燃烧生成CO2和液态水所放出的热量比顺-2-丁烯的大 |
| C、28 g顺-2-丁烯完全氢化生成丁烷气体时所放出的热量为118.9 kJ |
D、反-2-丁烯氢化的热化学方程式为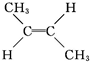 (g)+H2(g)→CH3CH2CH2CH3(g)△H=-112.7 kJ?mol-1 (g)+H2(g)→CH3CH2CH2CH3(g)△H=-112.7 kJ?mol-1 |
据下列反应判断有关物质的氧化性顺序正确的是( )
①F2+2NaCl(熔融)═2NaF+Cl2 ②Cl2+2NaBr═2NaCl+Br2 ③Br2+2NaI═2NaBr+I2.
①F2+2NaCl(熔融)═2NaF+Cl2 ②Cl2+2NaBr═2NaCl+Br2 ③Br2+2NaI═2NaBr+I2.
| A、F2>Br2>I2>Cl2 |
| B、I2>Br2>Cl2>F2 |
| C、F2>Cl2>Br2>I2 |
| D、NaI>NaBr>NaCl>NaF |
在世界海运史上曾发生过这样一个悲剧:一艘名叫“阿那吉纳号”的货轮满载着精铜砂,在向日本海岸行驶时突然发生大面积漏水,最终沉没.坚硬的钢制船体为什么会突然漏水呢?事后的事故调查结果表明导致沉船的原因与船上的精铜砂密切相关.下列对此调查结论的理解正确的是( )
| A、精铜砂装载过多导致沉船 |
| B、运输途中铜与空气中的氧气发生氧化反应导致质量增大超过船的承载能力 |
| C、在潮湿的环境中,船体与铜构成了原电池,加速了作为负极的船体的腐蚀 |
| D、在潮湿的环境中,船体与铜构成了电解池,钢制船体作阳极而被氧化腐蚀 |
 二甲醚(CH3OCH3)是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用.工业上以CO和H2为原料生产二甲醚CH3OCH3的新工艺主要发生三个反应:
二甲醚(CH3OCH3)是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用.工业上以CO和H2为原料生产二甲醚CH3OCH3的新工艺主要发生三个反应: